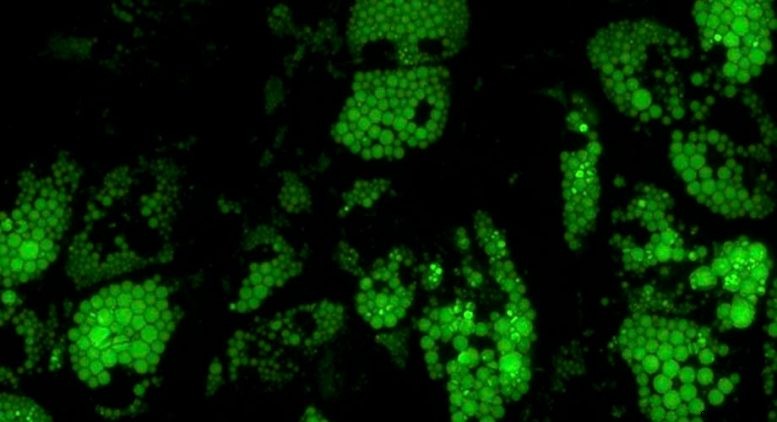
Zdrowe brunatne komórki tłuszczowe (pokazane na zielono) wymagają dużej ilości cząsteczki zwanej hemem, która umożliwia organizmowi prawidłowy metabolizm pokarmu. Laboratorium Saez w Scripps Research opisało, w jaki sposób ten ważny, ale bardzo toksyczny metabolit jest bezpiecznie transportowany wewnątrz komórek. Źródło:Scripps Research
Mało znane białko jest zwykle bogate w tłuszcz; bez niego organizm ma trudności z zarządzaniem glukozą i insuliną.
Dzięki nieoczekiwanym odkryciom dotyczącym białka, które ma wysoką ekspresję w tkance tłuszczowej, naukowcy ze Scripps Research otworzyli drzwi do krytycznego nowego zrozumienia otyłości i metabolizmu. Ich odkrycie, które zostało opublikowane dzisiaj (20 listopada 2019 r.) w czasopiśmie Nature , może prowadzić do nowych podejść do walki z otyłością i potencjalnie wieloma innymi chorobami.
Białko sygnałowe, znane jako PGRMC2, nie było w przeszłości intensywnie badane. Skrót od „składnik błonowy receptora progesteronu 2”, został wykryty w macicy, wątrobie i kilku obszarach ciała. Ale laboratorium dr Enrique Saeza zauważyło, że jest ono najbardziej obfite w tkankę tłuszczową – szczególnie w brązowy tłuszcz, który zamienia jedzenie w ciepło, aby utrzymać temperaturę ciała – i zainteresowało się jego funkcją w tym miejscu.
Ważna rola:przewodnik turystyczny Heme
Zespół oparł się na swoim ostatnim odkryciu, że PGRMC2 wiąże się i uwalnia niezbędną cząsteczkę zwaną hemem. Ostatnio w centrum uwagi ze względu na swoją rolę w nadawaniu smaku roślinnym Impossible Burger, hem odgrywa znacznie ważniejszą rolę w organizmie. Cząsteczka zawierająca żelazo przemieszcza się w komórkach, aby umożliwić kluczowe procesy życiowe, takie jak oddychanie komórkowe, proliferacja komórek, śmierć komórek i rytmy dobowe.
Korzystając z technik biochemicznych i zaawansowanych testów w komórkach, Saez i jego zespół odkryli, że PGRMC2 jest „opiekuńczym” hemu, zamykając cząsteczkę i transportując ją z mitochondriów komórki, gdzie powstaje hem, do jądra, gdzie pomaga Funkcje. Bez ochronnego opiekuna hem reagowałby ze wszystkim i niszczył wszystko na swojej drodze.
„Znaczenie Heme dla wielu procesów komórkowych jest znane od dawna”, mówi Saez, profesor nadzwyczajny na Wydziale Medycyny Molekularnej. „Ale wiedzieliśmy również, że hem jest toksyczny dla otaczających go materiałów komórkowych i będzie potrzebował jakiejś ścieżki wahadłowej. Do tej pory było wiele hipotez, ale białka, które przemycają hem, nie zostały zidentyfikowane”.
Innowacyjne podejście do otyłości?
Dzięki badaniom na myszach naukowcy ustalili PGRMC2 jako pierwszy wewnątrzkomórkowy hem opiekuńczy opisany u ssaków. Jednak na tym nie poprzestali; starali się dowiedzieć, co dzieje się w organizmie, jeśli to białko nie istnieje, aby transportować hem.
I tak dokonali kolejnego wielkiego odkrycia:bez PGRMC2 obecnego w ich tkankach tłuszczowych, myszy karmione dietą wysokotłuszczową stały się nietolerancyjne na glukozę i niewrażliwe na insulinę – charakterystyczne objawy cukrzycy i innych chorób metabolicznych. Natomiast myszy z otyłością i cukrzycą, którym podawano lek aktywujący funkcję PGRMC2 wykazały znaczną poprawę objawów związanych z cukrzycą.
„Widzieliśmy, że myszy poprawiają się, stają się bardziej tolerancyjne na glukozę i mniej odporne na insulinę” – mówi Saez. „Nasze odkrycia sugerują, że modulowanie aktywności PGRMC2 w tkance tłuszczowej może być użytecznym podejściem farmakologicznym do odwrócenia niektórych poważnych skutków zdrowotnych otyłości”.
Zespół ocenił również, w jaki sposób białko zmienia inne funkcje brązowego i białego tłuszczu, mówi główny autor badania, dr Andrea Galmozzi. „Pierwszym zaskakującym odkryciem było to, że brązowy tłuszcz wyglądał na biały” – mówi.
Tłuszcz brązowy, który zwykle ma najwyższą zawartość hemu, jest często uważany za „dobry tłuszcz”. Jedną z jego kluczowych ról jest generowanie ciepła w celu utrzymania temperatury ciała. Wśród myszy, które nie były w stanie wytwarzać PGRMC2 w tkankach tłuszczowych, temperatura szybko spadała po umieszczeniu w zimnym środowisku.
„Mimo że ich mózg wysyłał odpowiednie sygnały, aby włączyć ogrzewanie, myszy nie były w stanie obronić temperatury ciała” – mówi Galmozzi. „Bez hemu dochodzi do dysfunkcji mitochondriów, a komórka nie ma możliwości spalania energii w celu wytworzenia ciepła”.
Saez uważa, że aktywacja białka opiekuńczego hemu w innych narządach – w tym w wątrobie, gdzie wytwarzana jest duża ilość hemu – może pomóc złagodzić skutki innych zaburzeń metabolicznych, takich jak niealkoholowe stłuszczeniowe zapalenie wątroby (NASH), które jest główną przyczyną transplantacji wątroby dzisiaj.
„Jesteśmy ciekawi, czy to białko pełni tę samą rolę w innych tkankach, w których widzimy defekty hemu, które prowadzą do choroby” – mówi Saez.
###
Odniesienie:„PGRMC2 jest wewnątrzkomórkowym chaperonem hemu krytycznym dla funkcji adipocytów” Andrea Galmozzi, Bernard P. Kok, Arthur S. Kim, J. Rafael Montenegro-Burke, Jae Y. Lee, Roberto Spreafico, Sarah Mosure, Verena Albert, Rigo Cintron-Colon, Cristina Godio, William R. Webb, Bruno Conti, Laura A. Solt, Douglas Kojetin, Christopher G. Parker, John J. Peluso, James K. Pru, Gary Siuzdak, Benjamin F. Cravat i Enrique Saez, 20 Listopad 2019, Przyroda .
DOI:10.1038/s41586-019-1774-2
Praca była wspierana przez granty National Institutes of Health (DK099810, DK114785, DK121196, S10OD016357, OD016564). Dwóch badaczy, Kok i Albert, było również wspieranych przez stypendia American Heart Association.
