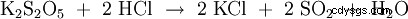| wzór strukturalny | |||||||
|---|---|---|---|---|---|---|---|
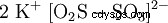 | |||||||
| Ogólne | |||||||
| Nazwa | Dwusiarczyn potasu | ||||||
| Inne nazwy |
| ||||||
| Formuła molekularna | K2 S2 O5 | ||||||
| Numer CAS | 16731-55-8 | ||||||
| Krótki opis | bezbarwny (biały) proszek o zapachu dwutlenku siarki | ||||||
| Właściwości | |||||||
| Masa molowa | 222,33 g mol | ||||||
| Stan materii | naprawiono | ||||||
| Gęstość | 2,34 g/cm | ||||||
| Temperatura topnienia | 190 °C (rozkład) | ||||||
| Temperatura wrzenia | Nie dotyczy | ||||||
| Rozpuszczalność | 450 g/l (20 ºC) w wodzie, nierozpuszczalny w alkoholu | ||||||
| Instrukcje bezpieczeństwa | |||||||
| |||||||
| LD50 | 2300 mg/kg (doustnie, szczur) | ||||||
| WGK | 1 (lekko niebezpieczne dla wody) | ||||||
| Tam, gdzie jest to możliwe i powszechne, używane są jednostki SI. O ile nie zaznaczono inaczej, podane dane dotyczą standardowych warunków. | |||||||
Dwusiarczyn potasu (K2 S2 O5 ) lub pirosiarczyn potasu , Pirosiarczyn potasu nazywana jest solą potasową kwasu dwusiarkowego, która nie jest stabilna w postaci wolnej. Dwusiarczyny mają dość długie, niestabilne wiązanie siarka-siarka. Dwusiarczyn potasu jest stosowany głównie jako środek konserwujący (E 224) w przemyśle spożywczym. W kwaśnych warunkach związek oddziela dwutlenek siarki:
Uzyskiwanie i wyświetlanie
Powstaje w wyniku termicznej dimeryzacji (kondensacji) wodorosiarczynu potasu z eliminacją wody (1) lub w reakcji dwutlenku siarki i siarczynu potasu w roztworze wodorotlenku potasu (2):
- (1)
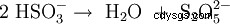
- (2)
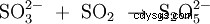
Wykorzystanie
Dodatek do żywności dwusiarczyn potasu (E 224) jest stosowany jako konserwant, przeciwutleniacz i stabilizator barwy żywności (np. również przy siarkowaniu wina).
Jest również powszechnie stosowany jako reduktor w przemyśle chemicznym, do bielenia cukru, jako środek kaustyczny w przemyśle elektronicznym oraz jako składnik utrwalaczy w przemyśle fotograficznym.
Referencje
- ↑ hazard-materials-data.de [1]
- ↑ nieorganiczny.basf.com [2]
- ↑ Merck - ChemDAT.info [3]
- ↑ metalograf.de [4]