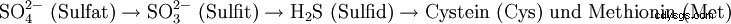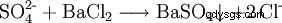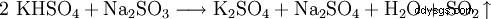| Eigenschaften | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Allgemein | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom, Symbole, Ordnungszahl | Schwefel, S, 16 ans | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Série | Nichtmetalle | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe, Période, Bloc | 16, 3, p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aussehen | zitronengelb | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massenanteil an der Erdhülle | 0,05 % | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atommasse | 32 065 unités | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomradius (berechnet) | 100 (88) h | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de Kovalenter | 22h | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de Van-der-Waals | 180h | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuration électronique | [Ne] 3s 3p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronen pro Energieniveau | 2, 8, 6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Ionisierungsenergie | 999,6 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Ionisierungsenergie | 2252 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Ionisierungsenergie | 3357 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. Ionisierungsenergie | 4556 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5. Ionisierungsenergie | 7004,3 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6. Ionisierungsenergie | 8495,8 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Physique | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Agrégatzustand | fête | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modifications | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallstruktur | orthorhombisch | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dichte | 1,96 g/cm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mohshärte | 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnétisme | diamagnetisch | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzpunkt | 388,36 K (115,21 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Siedepunkt | 717,87 K (444,72 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molares Volumen | 15,53 · 10 m/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verdampfungswärme | 9,6 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schmelzwärme | 1,7175 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dampfdruck | 2,65 · 10 Pa à 388 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Schallgeschwindigkeit | m/s | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Spezifische Wärmekapazität | 710 J/(kg·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrische Leitfähigkeit | 5,0 · 10 S/m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wärmeleitfähigkeit | 0,269 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chimique | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxydationszustände | ±2, 4, 6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxyde (Basizität) | SO2 , SO3 (stark sauer) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Potentiel normal | -0,48 V (S + 2e → S) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électricité | 2,58 (Pauling-Skala) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotope | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eigenschaften RMN | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gefahrstoffkennzeichnung | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| R- et S-Sätze | R :11 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S :33 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Schwefel (chemisch nach dem Lateinischen Soufre [ˈzʊlfʊr] ou Soufre genannt, im Deutschen eventuell vom Indogermanischen *suel- „schwelen“ abgeleitet) ist ein chemisches Element der Sauerstoffgruppe. Er verbrennt an der Luft mit blauer Flamme und erzeugt dabei stechend riechendes Schwefeldioxid. Schwefel ist für Lebewesen ein Essential Element. Er kommt unter anderem in Aminosäuren und Enzymen vor, und spielt eine wichtige Rolle bei der anaeroben Energiegewinnung vieler Mikroorganismen.
Modifications
Schwefel tritt in verschiedenen Modifikationen auf :
Fester Schwefel
- Die bei Raumtemperatur thermodynamisch stabilste Modifikation des Schwefels ist α-Schwefel, rhombisch kristallisierend (rhombischer Schwefel). Er ist geruch- und geschmackslos und hat die typische schwefelgelbe Farbe.
- Bei 95,6 °C liegt der Umwandlungspunkt zu β-Schwefel. Diese Schwefelmodifikation ist fast farblos und kristallisiert monoklin (monokliner Schwefel).
- Seltener ist der ebenfalls monoklin kristallisierende γ-Schwefel (Rosickyit).
Flüssiger Schwefel
- λ-Schwefel :S8 -Ringe (gelb) (Schwefelblüte)
- π-Schwefel :Sn (6 ≤ n ≤ 25, n ≠ 8) niedermolekulare und größere Ringe
- μ-Schwefel :Sn (10 ≤ n ≤ 10) hochmolekulare Ketten
Fester Schwefel besteht normalerweise aus S8 -Molekülen, bei denen acht Schwefel-Atome in einem Ring zick-zack-förmig gebunden sind (sog. Kronenform). Beim Erhitzen schmilzt der β-Schwefel, wobei auch andere Ringe (v. a. S6 , S7 , S12 ) in temperaturabhängigen Anteilen auftreten. Bei weiterer Erhöhung der Temperatur brechen die Ringe durch thermische Anregung auf und zunächst lange Ketten (Polymérisation, sog. λ-Übergang bei ca. 159 °C), diese verkürzen sich durch Zerfall dann bei steigender Temperatur wieder. Neben diesen Schwefelketten liegen aber immer auch S-Ringe vor, im wesentlichen jedoch S8 . Am λ-Übergang ändern sich eine Reihe physikalischer Eigenschaften (z. B. Viskosität, optische Absorption und damit auch die Farbe).Gasförmiger Schwefel ist dunkelrot und besteht anfangs aus S8 -Ringen, die bei höheren Temperaturen dann weiter aufbrechen, so dass die Moleküle immer kleiner werden. Ab etwa 1800 °C hat man dann Schwefelatome.
Vorkommen
Schwefel kommt mit einem Anteil von 0,048 % in der Erdhülle (15. Stelle der Elementhäufigkeit) vor. In der Natur kommt Schwefel elementar in mächtigen Lagerstätten z.B. au Sizilien, en Pologne, en Irak, en Iran, en Louisiane, au Texas et au Mexique.
Weitverbreitet ist Schwefel in sulfidischen Mineralien, wie Pyrit FeS2 , Kupferkies CuFeS2 , Bleiglanz PbS et Zinkblende ZnS. Die meisten Metalle (v.a. Schwermetalle) kommen in der Natur als schwerlösliche Sulfide vor.
Auch in Form von Sulfaten, wie Gips (CaSO4 · 2 H2 O), Schwerspat (BaSO4 ) oder anderen schwer wasserlöslichen Sulfaten kommt Schwefel natürlich vor.
Eine wichtige Quelle für Schwefel sind fossile Brennstoffe wie Erdöl, Erdgas und Kohle. Vor allem Erdgas enthält relativ viel Schwefelwasserstoff (H2 S). Es ist darin durch Abbau schwefelhaltiger organischer Stoffe entstanden.
Schwefel comme minéral
Schwefel tritt gediegen, également sous forme élémentaire, en tant que Schwefelblüte (Gelber Schwefel ) in der Natur auf. Er kristallisiert unterhalb etwa 95 °C im orthorhombischen Kristallsystem (α-Schwefel), hat eine Dichte von 2,0 bis 2,1, eine Härte von 1,5 bis 2,5 und eine hell- bis dunkelgelbe Farbe, sowie eine weiße Strichfarbe . Meist zeigt er hellgelbe prismen- oder pyramidenförmige Kristalle, die sich auf Gesteinsflächen aus schwefelreichen Gasen durch unvollständige Oxidation von Schwefelwasserstoff (H2 S) ou Reduktion von Schwefeldioxid (SO2 ) photos. Oberhalb etwa 95 °C kristallisiert Schwefel monoklin (β-Schwefel). Diese Form wandelt sich unterhalb 95 °C rasch in die orthorhombische α-Form um.
Reiner Schwefel ist relativ selten, wird allerdings in großen Mengen bei Vulkanausbrüchen freigesetzt. Er findet sich in Vulkanschloten oder an anderen Postvulkanischen Erscheinungen.Schwefel kommt aber auch in derber Form, das heißt, ohne mit bloßem Auge erkennbare Kristalle vor, insbesondere in Sedimenten oder Sedimentgesteinen. Häufig findet er sich in Evaporiten (Salzgesteinen), wo er meistens durch Reduktion von Sulfaten entsteht.
Charakteristisch für das Mineral sind neben der geringen Härte die Farbe und der niedrige Schmelzpunkt 112,8 °C (α-S) beziehungsweise 119,2 °C (β-S).Siedepunkt bei 444,7 °C
Gewinnung
Früher bildete das gediegene Mineral eine wichtige Quelle für Schwefel:3,5 Millionen Tonnen wurden jährlich mit Hilfe des von Hermann Frasch entwickelten Frasch-Verfahrens abgebaut, hauptsächlich in den USA und in Polen. Den größten Anteil machte jedoch aus Sulfiderzen gewonnener Schwefel aus:Aus dieser Quelle stammten etwa 50 Millionen Tonnen pro Jahr. Heute fällt der Schwefel in großen Mengen als Abfallprodukt bei der Entschwefelung von Erdöl mit Hilfe des Claus-Verfahrens an.
Biologische Bedeutung
Schwefel ist in den Aminosäuren Cystein und Methionin − und in allen darauf aufbauenden Polypeptiden, Proteinen und Enzymen − enthalten. Schwefel ist damit ein Element essentiel lebender Zellen. Disulfidbrückenbindungen sind weit verbreitet und tragen zur Ausbildung und Stabilisierung von Proteinstrukturen bei.
Einige Untergruppen der Proteobakterien sind in der Lage, unter Sauerstoffausschluss Photosynthese zu betreiben. Sie verwenden Schwefelwasserstoff (H2 S) oder elementaren Schwefel an Stelle von Wasser (H2 O) als Elektronendonator für die Reduktion von CO2 , siehe dazu exemplarisch Thiomargarita namibiensis .
Pflanzen nehmen Schwefel über die Wurzeln in Form von Sulfat-Ionen auf, die dann zu Sulfid reduziert und anschließend zur Bildung von Cystein und anderen organischen Schwefelverbindungen genutzt werden.
Schwefel-Assimilation à Pflanzen
Der Schwefel wird als Sulfat über die Wurzeln aufgenommen. Die Assimilation findet zwar auch in den Wurzeln statt, die Hauptmenge des Sulfats wird jedoch über die Xylemelemente in die Blätter transportiert und dort im Chloroplasten reduziert :
Ökologische Aspekte
Bei der Energiegewinnung aus fossilen Brennstoffen wie Steinkohle, Braunkohle und Erdöl werden große Mengen Schwefeldioxid SO2 freigesetzt. Dieses bleibt als Gas oder im Wasser der Wolken gelöst zunächst in der Atmosphäre. Dabei bildet es einen wichtigen Bestandteil des gesundheitsgefährdenden Smogs. Abgebaut werden kann es, indem von Sauerstoff zu Schwefeltrioxid SO3 oxidiert wird und dann als Schwefelsäure H2 SO4 mit dem Regen ausgespült wird. Daraus ergibt sich ein weiteres Problem, da diese als Bestandteils des Sauren Regens zur Versauerung der Böden beiträgt. Seit den 1970er Jahren sind darum Maßnahmen zur Rauchgasentschwefelung in Deutschland gesetzlich vorgeschrieben. Daneben werden seit einigen Jahren die Entschwefelung von Fahrzeugkraftstoffen (vor allem Diesel) forciert. Durch diese Vorschriften und ihre Umsetzungen konnten die Schwefelemissionen seit den 1960er Jahren drastisch reduziert werden. Dies spiegelt sich auch deutlich in der Tatsache plus large, dass in der Landwirtschaft die Schwefeldüngung notwendig wird. Dies war zuvor nicht relevant.
Verwendung
Schwefel wird sowohl in der chemischen Industrie als auch in der pharmazeutischen Industrie genutzt, unter anderem zur Produktion von Schwefelsäure, Farbstoffen, Insektiziden und Kunstdüngern.
Der pharmazeutische Nutzen von Schwefel war bereits im Altertum bekannt. Innerlich wurde Schwefel als Laxans (Abführmittel) eingesetzt. Er reizt die Darmschleimhaut. Der dabei durch Bakterien erzeugte Schwefelwasserstoff regt die Peristaltik an. Äußerlich kamen Schwefelrezepturen bei Hauterkrankungen wie Akne, Ekzemen, Krätze, Mykosen u. un. zum Einsatz. Heute findet Schwefel in der Dermatologie nur noch selten Verwendung, ist aber noch nicht vollständig aus der pharmazeutischen Literatur verschwunden. Nach wie vor gibt es pharmazeutische Zubereitungen, die als Wirkbzw. Hilfsstoff Schwefel enthalten. In der klassischen Homöopathie ist Soufre eines der so genannten großen Mittel .
In der Schwerindustrie ist Schwefel als Legierungselement für Stahl bedeutend. Automatenstähle sind oft schwefellegiert, da Schwefel zu erhöhtem Spanbruch führt.
Schwefel findet auch bei der Herstellung von Schwarzpulver, als Salpeterschwefel in der Feuerwerkerei, oder bei anderen Explosivstoffen Verwendung.
Schwefelverbindungen
Sulfure
- Schwefelwasserstoff
- Sulfure, wie Zinnober (HgS)
- Wasserstoffpersulfide
Oxyde
- Schwefeloxide, wie Schwefeldioxid et Schwefeltrioxid,
Sauerstoffsäuren et Salze
| Säuren de Typus H2 SOn | ||||
|---|---|---|---|---|
| Oxydationsstufe des Schwefels | Structure | Sauren | Salze | Beispiele |
| +II | Sulfoxylsäure H2 SO2 | Sulfoxylate | ||
| +IV | Schweflige Säure H2 SO3 | Sulfite |
| |
| +VI | Schwefelsäure H2 SO4 | Sulfate |
| |
| +VI | Peroxo(mono)schwefelsäure H2 SO5 | Peroxosulfate |
| |
| Säuren de Typus H2 S2 On | ||||
|---|---|---|---|---|
| mttlere Oxidationsstufe des Schwefels | Structure | Sauren | Salze | Beispiele |
| +je | Thioschwefelige Säure H2 S2 O2 | Thiosulfite (unbekannt) | ||
| +II | Thioschwefelsäure H2 S2 O3 | Thiosulfate |
| |
| +III | Dithionige Säure H2 S2 O4 | Dithionite |
| |
| +IV | Dischweflige Säure H2 S2 O5 | Disulfite |
| |
| +V | Dithionsäure H2 S2 O6 | Dithionate |
| |
| +VI | Dischwefelsäure H2 S2 O7 | Disulfate | ||
| +VI | Peroxodischwefelsäure H2 S2 O8 | Peroxodisulfate |
| |
Nitrure
- Nitrure de Schwefel :S4 N4 , S2 N2 et (SN)x
Halogénure
- Schwefelhalogénure :z. B. Schwefeldichlorid, Schwefeltetrachlorid, Dischwefeldichlorid und höhere Oligosulfanchloride (Vulkanisierung)
Organoschwefelverbindung
In zahlreichen organischen Verbindungen kommt Schwefel gebunden vor und wird unter Organoschwefelverbindung ausführlicher beschrieben.
- Thiole (=Mercaptane)
- Thioéther
- Heterocyclische Verbindungen, wie Thiophen
- Sulfoxide wie Dimethylsulfoxid als Lösungsmittel
- Sulfone
- Sulfonsäuren, deren Salze, die Sulfonate, zum Beispiel als Tenside dienen
Nachweis
Es existentieren verschiedene Nachweisreaktionen für Schwefel. Schwefel wird in Verbindungen nach Reduktion durch elementares Natrium in Natriumsulfid überführt. Sulfid-Anionen weist man mit Blei-II-salzlösungen nach, wobei ein schwarzer Niederschlag von Blei-II-sulfid entsteht :
Beim Ansäuern von festen, également ungelösten Sulfiden entsteht zudem ein charakteristischer Geruch, nach faulen Eiern (Verdrängungsreaktion, Vorsicht :Das Gas Schwefelwasserstoff ist giftig; Einatmen vermeiden, Abzug !). Auch dieses Gas schwärzt Bleiacetatpapier.
Durch Oxydation schwefelhaltiger Verbindungen entstehen Sulfit und Sulfat. Letzteres weist man mit Barium-II-salzlösungen nach :Es entsteht ein weißer Niederschlag von Bariumsulfat :
Sulfit wird mit Kaliumhydrogensulfat nachgewiesen. Beim Verreiben der auf Sulfit zu prüfenden Substanz mit Kaliumhydrogensulfat entsteht das stechend riechende Schwefeldioxid. Für Natriumsulfit ergibt sich folgende Reaktiongleichung:
Anecdotes
- Bei den mittelalterlichen Alchemisten symbolisierte der Löwe den Schwefel
- Nicht nur in der deutschen Literatur wird der Geruch von Schwefel meist mit dem Erscheinen des Teufels assoziiert, bzw. kündigt Schwefelgeruch den Teufel an (vgl. auch die Rede von Hugo Chavez vor der UNO ).
Quellen
- ↑ Sicherheitsdatenblatt (alfa-aesar)
- ↑ Holleman-Wiberg :Lehrbuch der Anorganischen Chemie 102. Auflage, de Gruyter, Berlin, 2007.
- ↑ Der Spiegel, 20.09.2006[1]
- Systematik der Minerale
- Liste des minéraux
Littérature
- R. Steudel (Hrsg.) :Soufre élémentaire et composés riches en soufre (partie I et II). Dans :Sujets en chimie actuelle. Vol. 230 &231, Springer, Berlin 2003
| H | Il | ||||||||||||||||||||||||||||||
| Li | Être | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | Comme | Se | Br | Kr | ||||||||||||||
| Rb | Sr | Oui | Zr | Nb | Mois | TC | Ru | Rh | Pd | Ag | CD | Dans | Sn | Sb | Té | Je | Xe | ||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Euh | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | À | Rn |
| En | Ra | Ac | Th | Pa | U | Np | Pu | Suis | cm | Noir | Cf | Es | Fm | Md | Non | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Ub | Uut | Uuq | Oup | Euh | Uus | Uuo |
| Métal alcalin | Erdalkalimétalle | Lanthanoïde | Actinoide | Übergangsmetalle | Métal | Halbmetalle | Nichtmetall | Halogène | Edelgase |