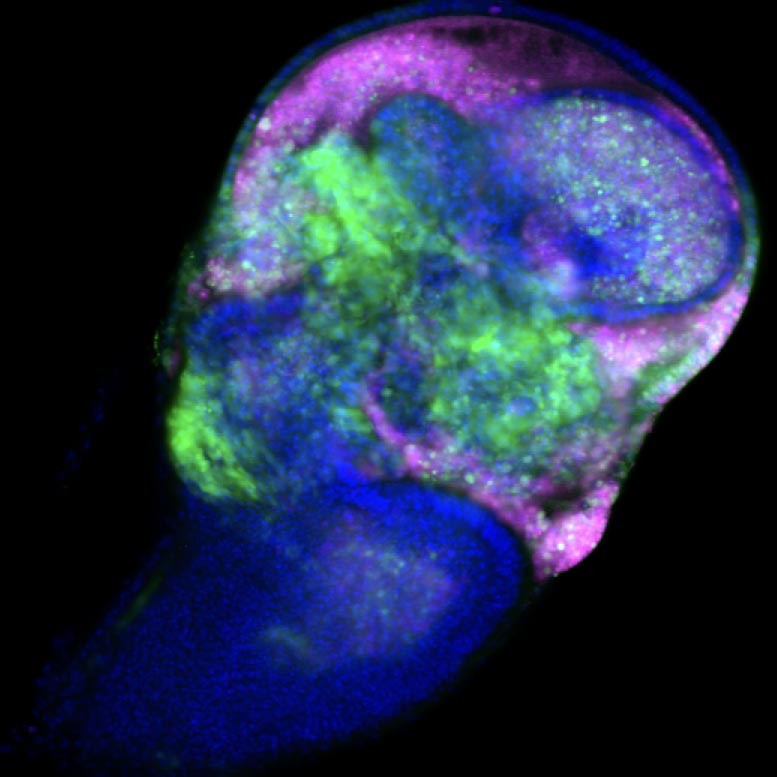
To zdjęcie przedstawia wyimaginowany dysk skrzydła muszki owocowej. Zielone komórki to żywe i proliferujące komórki, które wyrażają onkogen Src. Komórki magenta to komórki umierające z powodu ekspresji Src. Tak więc Src promuje jednocześnie proliferację (zielony) i śmierć komórki (magenta). Źródło:RIKEN
Grupa badawcza w RIKEN Center for Biosystems Dynamics Research (BDR) odkryła zdarzenia molekularne, które decydują o tym, czy komórki rakowe żyją, czy umierają. Dzięki tej wiedzy odkryli, że zmniejszone spożycie określonego bloku budulcowego białka zapobiega wzrostowi komórek, które stają się rakowe. Te odkrycia zostały opublikowane w czasopiśmie naukowym eLife i otworzyć możliwość terapii dietetycznej na raka.
Guz to grupa komórek rakowych, które namnażają się – lub proliferują – w sposób niekontrolowany. Nowotwory powstają z pojedynczych komórek, które stają się rakowe, gdy geny powodujące proliferację komórek są nadmiernie aktywowane. Ponieważ jednak te geny, zwane onkogenami, często powodują również śmierć komórki, aktywacja pojedynczego onkogenu w komórce nie wystarczy, aby stał się on komórką rakową. Uważa się, że to zjawisko jest „bezpiecznym w przypadku awarii” mechanizmem, który zapobiega łatwemu przekształcaniu się komórek w raka. Aby komórka prześlizgnęła się przez pęknięcia i stała się rakiem, kilka innych onkogenów, wraz z genami hamującymi nowotwór, musi zostać aktywowanych w wieloetapowym procesie. Szczegóły tego procesu były tematem nowego badania.
Międzynarodowa grupa badawcza kierowana przez Sa Kan Yoo z RIKEN BDR skupiła się na onkogenie Src i zbadała, w jaki sposób proliferacja komórek – onkogeneza – i śmierć komórek są regulowane u muszki owocowej. Wykazali, że Src nie indukuje śmierci komórki w wyniku proliferacji komórek, lecz napędza oba procesy niezależnie i jednocześnie. Hamując funkcję określonych genów poprzez interferencję RNA, zespół odkrył, że gen p38 był zaangażowany w proliferację komórek, a gen JNK był zaangażowany w śmierć komórki. Ponadto odkryli gen zwany slpr, który jednocześnie aktywuje p38 i JNK. „Sposób, w jaki onkogeny jednocześnie promują śmierć i proliferację komórek, budzi kontrowersje” – mówi Yoo. „Naszym głównym odkryciem było to, że onkogen Src promuje śmierć i proliferację komórek poprzez równoległe ścieżki”.
Jedna koncepcja leczenia raka wykorzystuje mechanizm „fail-safe” poprzez hamowanie proliferacji komórek, ale nie śmierci komórki. Aby to zrobić, musimy znać molekularnych graczy zaangażowanych w ten proces. Gdy zespół zidentyfikował aktywację p38 jako kluczowy krok prowadzący do proliferacji komórek, zdali sobie sprawę, że mogą urzeczywistnić tę koncepcję. Po przestudiowaniu tego, co jeszcze wiemy o p38, zdali sobie sprawę, że jego aktywność może być kontrolowana przez składniki odżywcze w diecie.
Następnie postanowili przetestować tę hipotezę, badając związek między pokarmem podawanym larwom much a proliferacją komórek. Odkryli, że zmniejszenie ilości aminokwasu metioniny w diecie zapobiegało onkogenezie kontrolowanej przez p38. „Byliśmy podekscytowani odkryciem, że manipulowanie ilością metioniny w diecie może wpływać na proliferację komórek, ale nie na ich śmierć” – mówi Yoo. „Obecnie nie wiemy, czy nasze odkrycie u much przełoży się na przypadki raka u ludzi. Spekulujemy jednak, że będzie to miało miejsce w szczególnych przypadkach, ponieważ niektóre nowotwory u ludzi również aktywują gen Src.
„Jesteśmy ciekawi, jak ogólny jest mechanizm, który tu znaleźliśmy. Poza szlakiem sygnalizacyjnym Src odkryliśmy również, że slpr może pośredniczyć w szlakach sygnalizacyjnych kontrolowanych przez inne onkogeny. Dowiedzenie się, jak to się dzieje, jest naszym następnym celem”.
Ponieważ wiadomo, że proces onkogenezy jest taki sam zarówno u muszek owocowych, jak i ssaków, nowe odkrycia mogą pomóc wyjaśnić, w jaki sposób rozwijają się nowotwory u ludzi.
Odniesienie:„Ograniczenie metioniny przerywa obowiązkowe sprzężenie proliferacji komórek i śmierci przez onkogen Src w Drosophila” Hiroshi Nishida, Morihiro Okada, Lynna Yang, Tomomi Takano, Sho Tabata, Tomoyoshi Soga, Diana M Ho, Jongkyeong Chung, Yasuhiro Minami i Sa Kan Yoo, 27 kwietnia 2021 r., eLife.
DOI:10.7554/eLife.59809
