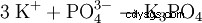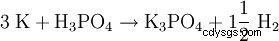| formula strutturale | |||||||
|---|---|---|---|---|---|---|---|
| 3 K | |||||||
| Generale | |||||||
| Nome | fosfato di potassio | ||||||
| Altri nomi | fosfato tripotassico | ||||||
| Formula molecolare | K3 PO4 | ||||||
| Numero CAS | 7778-53-2 | ||||||
| Proprietà | |||||||
| Massa molare | 212,28 g mol | ||||||
| Stato della materia | risolto | ||||||
| Densità | 2,56 kg m | ||||||
| Punto di fusione | 1340 °C | ||||||
| Solubilità | solubile in acqua | ||||||
| Istruzioni di sicurezza | |||||||
| |||||||
| Ove possibile e comune, vengono utilizzate le unità SI. Salvo diversa indicazione, i dati forniti si applicano a condizioni standard. | |||||||
fosfato di potassio è il sale di potassio dell'acido fosforico.
Ottenere/Rappresentare
Il fosfato di potassio si forma anche quando le scorie di Thomas vengono riscaldate con carbone e solfato di potassio.
Proprietà
Il fosfato di potassio si dissolve in acqua con reazione alcalina.
Produzione:
Utilizzo
I fosfati sono usati come additivi nei detersivi, sono in grado di ridurre la durezza dell'acqua formando complessi con ioni metallici multivalenti (Mg ecc.). Il loro utilizzo è ora vietato in alcuni paesi (compresa la Svizzera).
I fosfati sono anche usati come fertilizzanti artificiali.
Importanza biologica
La conseguenza del suo utilizzo nei detergenti è un maggiore apporto di nutrienti nei corpi idrici. Ciò si traduce in una maggiore crescita delle alghe, che può portare al ribaltamento di uno specchio d'acqua.
Il fosfato di potassio è noto in omeopatia come agente nervino.