Obésité :une réponse immunitaire dangereuse
Une alimentation malsaine entraîne une activation fatale des cellules immunitaires. Une équipe de chercheurs du LMU, en collaboration avec la Harvard Medical School de Boston, a découvert de nouvelles influences moléculaires.
Selon l'Organisation mondiale de la santé (OMS), le surpoids et l'obésité figurent parmi les plus grands problèmes de santé du 21e siècle. Près de 60 % des Allemands sont considérés en surpoids, tandis que 25 % sont obèses. De plus, le surpoids déclenche souvent des maladies secondaires graves telles que le diabète, l'artériosclérose ou les crises cardiaques.
Ce qui trouble les médecins, c'est la taille du tissu adipeux dans l'abdomen - ou du tissu adipeux viscéral, pour être technique. Une forte expansion de ce tissu est associée à une réponse immunitaire inflammatoire qui englobe tout le corps et augmente ainsi le risque de maladies secondaires. Le tissu adipeux viscéral joue un rôle important dans ces processus :les cellules immunitaires peuvent alors s'organiser en structures lymphoïdes et déclencher des réponses immunitaires qui font dérailler le métabolisme de la personne.
Le régime est la clé
Une équipe de chercheurs du LMU a maintenant étudié les processus moléculaires qui influencent ce soi-disant immunométabolisme. Ils ont constaté que l'alimentation joue un rôle décisif :« Après seulement trois semaines d'un régime riche en graisses et en calories, nous constatons des changements dans les processus moléculaires qui contrôlent le système immunitaire et le métabolisme dans l'organisme », explique le Dr Susanne Stutte. du Centre biomédical de Munich et auteur principal de l'étude. L'énergie alimentaire excédentaire est stockée dans le tissu adipeux, comme la graisse viscérale, qui est située dans l'abdomen et entre les organes internes. Bien que tout le monde possède cette graisse viscérale, une alimentation particulièrement calorique provoque son expansion et présente un risque pour la santé.
Avec la croissance constante de la graisse viscérale, les processus immunologiques deviennent déséquilibrés, comme les chercheurs ont pu le démontrer :un type particulier de cellules immunitaires appelées cellules dendritiques plasmacytoïdes (pDC) s'accumule dans le tissu adipeux viscéral. "Le tissu lymphoïde tertiaire commence à se former, dans lequel les pDC orchestrent le système immunitaire et influencent le métabolisme", explique Stutte.
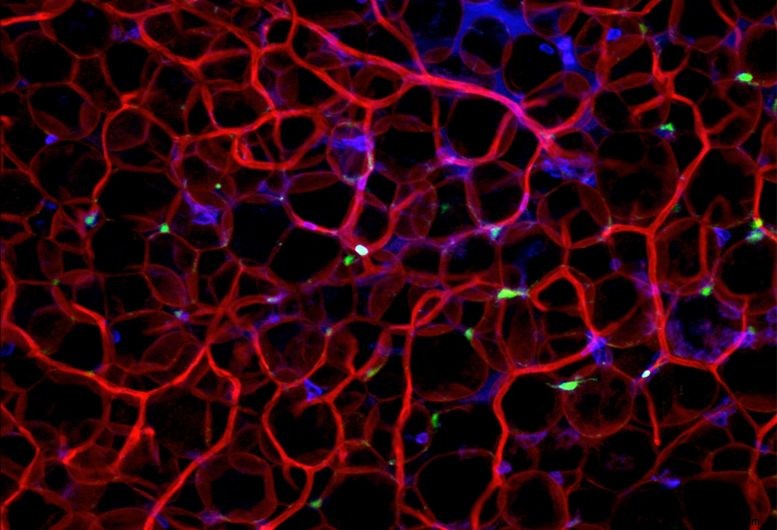
Vasculature dans le tissu adipeux viscéral murin (rouge :vaisseaux sanguins, vert :pDC, bleu :cellules hématopoïétiques). Crédit :LMU
Inflammation chronique
Lorsque le tissu adipeux se dilate, ces structures se forment à un rythme croissant. Désormais, les pDC interviennent de manière aiguë dans le métabolisme, créant un syndrome métabolique car les pDC de la graisse viscérale sont en état d'alerte constant.
"Les pDC représentent généralement la première barrière en cas d'infection virale, à laquelle elles répondent en libérant un messager (interféron de type I) qui instruit le système immunitaire", explique le professeur Barbara Walzog du Walter Brendel Center of Experimental Medicine au LMU et responsable du Centre de Recherche Collaborative SFB 914 "Trafficking of Immune Cells in Inflammation, Development and Disease."
Lorsque les marqueurs inflammatoires augmentent, le métabolisme déraille et le syndrome métabolique survient. "Lorsque la migration des pDC dans la graisse est bloquée, la prise de poids est réduite et l'état métabolique s'améliore", rapporte Stutte.
Cartes moléculaires
L'étude a été réalisée en collaboration avec la Harvard Medical School, et de l'avis des chercheurs, les résultats pourraient contribuer au développement de nouvelles approches vers une intervention thérapeutique dans les maladies métaboliques. La migration des pDC dans le tissu adipeux suit des modèles moléculaires exacts, qui peuvent être conçus comme des cartes. "Si nous pouvions arrêter la migration des pDC dans la graisse, par exemple, nous pourrions également prévenir les maladies secondaires qui en résultent", explique Walzog.
Référence :"Le régime riche en graisses modifie rapidement le trafic, le phénotype et la fonction des cellules dendritiques plasmacytoïdes dans le tissu adipeux" par Susanne Stutte, Hellen Ishikawa-Ankerhold, Lydia Lynch, Sarah Eickhoff, Simona Nasiscionyte, Chenglong Guo, Dominic van den Heuvel, Daniel Setzensack, Marco Colonna, Daniela Maier-Begandt, Ludwig Weckbach, Thomas Brocker, Christian Schulz, Barbara Walzog et Ulrich von Andrian, 15 mars 2022, The Journal of Immunology .
DOI :10.4049/jimmunol.2100022
