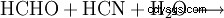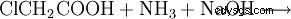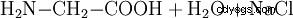| fórmula estructural | ||
|---|---|---|
| General | ||
| nombre | Glicina | |
| Abreviatura | Gly, G | |
| Restname | glicilo | |
| esencial | no | |
| Otros nombres | Glicol, glicol, ácido aminoacético | |
| Fórmula molecular | C2 H5 NO2 | |
| Número CAS | 56-40-6 | |
| Breve descripción | blanco sólido | |
| Propiedades | ||
| Masa molar | 75,07 g/mol | |
| Estado de la materia | arreglado | |
| Densidad | 1,595 g/cm | |
| Punto de fusión | 450-500 °F | |
| Punto de ebullición | > 230 °C descomposición térmica | |
| Presión de vapor | Pa (°C) | |
| cadena lateral | sin cadena lateral, de lo contrario hidrofílico | |
| Solubilidad | bueno en agua (225 g/l a 20 °C), pobre en alcohol, insoluble en disolventes no polares | |
| punto isoeléctrico | 6.06 | |
| Valores de pK a 25 °C | pKCOOH :2,4 pKNH2 :9,8 | |
| volumen de van der Waals | 48 | |
| Índice de hidrofobicidad | −0,4 | |
| Instrucciones de seguridad | ||
| ||
| Frases R y S | R:sin frases de riesgo S:sin frases S | |
| MAC | no establecido | |
| Donde sea posible y común, se utilizan unidades SI. A menos que se indique lo contrario, los datos proporcionados se aplican en condiciones estándar. | ||
Glicina (llamado químicamente ácido aminoacético), es el aminoácido proteinogénico más pequeño y simple. Pertenece al grupo de los aminoácidos hidrofílicos y es el único aminoácido proteinogénico que no es quiral y por lo tanto no es ópticamente activo.
La glicina no es esencial, por lo que puede ser producida por el propio organismo humano y es un componente importante de casi todas las proteínas y un nodo importante en el metabolismo.
El nombre deriva del sabor dulce de la glicina pura (del gr. glicis :Dulce).
Síntesis
La glicina se forma, entre otras cosas, en la reacción de formaldehído, cianuro de hidrógeno y agua:
Esta reacción es de particular importancia debido a la hipótesis de que los materiales de partida podrían haberse formado a partir de la llamada atmósfera primordial que rodeaba la tierra hace unos 4.000 millones de años. Tenía un presunto compuesto de hidrógeno (H2 ), helio (He) y en menor medida metano (CH4 ), amoníaco (NH3 ) y algunos otros gases nobles.
Químicamente, la glicina también se puede preparar a partir de ácido monocloroacético y amoníaco:
En el cuerpo, la mayor parte de la glicina se obtiene de los alimentos, pero también se puede producir a partir de la serina.
Funciones
Metabolismo
Además de producir glicina, la conversión de serina en glicina también sirve para convertir el ácido tetrahidrofólico en ácido N-N-metileno-tetrahidrofólico, que se requiere, entre otras cosas, para la síntesis de nucleótidos de timina (componente del ADN).
La glicina también se requiere directamente para la síntesis de otros componentes del material genético (purinas). También sirve para la biosíntesis de hemo (ligadura de oxígeno en la sangre), creatina (almacenamiento de energía en los músculos) o glutatión.
Como un llamado aminoácido glucogénico, la glicina se puede convertir en glucosa a través del piruvato como parte del metabolismo.
El ácido oxálico tóxico también se puede formar a partir de la glicina como subproducto.
Es particularmente común en el colágeno, la proteína más común en los organismos animales. Aquí representa un buen tercio de todos los aminoácidos, ya que su pequeño tamaño permite que el colágeno se enrolle en su estructura de triple hélice.
sistema nervioso
La glicina actúa en el sistema nervioso central a través del receptor de glicina como neurotransmisor inhibidor, es decir, como sustancia de señalización inhibidora. Actúa abriendo los canales de cloruro controlados por ligandos, lo que genera un potencial postsináptico inhibidor (IPSP), que reduce la actividad de las neuronas aguas abajo.
Las células nerviosas liberadoras de glicina (neuronas glicinérgicas) se encuentran principalmente en la médula espinal e inhiben las llamadas motoneuronas del asta anterior, lo que provoca una reducción de la actividad muscular de los músculos inervados por las células.
La estricnina, un antagonista del receptor de glicina, y la toxina tetánica, que inhibe la liberación de glicina, provocan una reducción del efecto de la glicina. La pérdida de la inhibición aumenta la actividad muscular. Esto puede provocar calambres potencialmente mortales.
Uso
La glicina se agrega a los alimentos como potenciador del sabor.
La glicina y su sal de sodio están numeradas E 640 como aditivo alimentario en la UE Generalmente aprobado para alimentos sin restricciones de cantidad máxima, los efectos sobre la salud no se conocen.
Referencias
- G. Löffler, P. E. Petrides:Bioquímica y patobioquímica , 7.ª edición, Springer Verlag, 2003, ISBN 3-540-42295-1