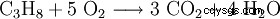| strukturformel | |||||||
|---|---|---|---|---|---|---|---|
| Allmänt | |||||||
| Namn | Propan | ||||||
| Molekylformel | C3 H8 | ||||||
| CAS-nummer | 74-98-6 | ||||||
| Kort beskrivning | färglös gas | ||||||
| Egenskaper | |||||||
| Molarmassa | 44,10 g/mol | ||||||
| Sakens tillstånd | gasformig | ||||||
| Densitet | 1,83 kg/m | ||||||
| Smältpunkt | -187,7 °C | ||||||
| Kokpunkt | -42 °C | ||||||
| Ångtryck | 7700hPa (20°C) | ||||||
| Löslighet | inte i vatten (0,08 g/l vid 20 °C) | ||||||
| Säkerhetsinstruktioner | |||||||
| |||||||
| MAK | 1000 ml/m | ||||||
| Där det är möjligt och vanligt används SI-enheter. Om inget annat anges gäller de angivna uppgifterna under standardvillkor. | |||||||
Propan är en färglös gas, den tillhör alkanerna, de enklaste kolvätena.
Egenskaper
Propan är en färglös och luktfri gas med en smältpunkt på -187,7 °C och en kokpunkt på -42 °C. Den kritiska punkten är vid 94 °C (369,82 K =96,67 °C enligt "Handbook of Chemistry and Physics" 76:e upplagan, 1995-1996) och 4,24 MPa. Så propan kan lätt göras flytande. Det löser sig mycket svagt vid 20 °C till 80 mg/l i vatten. Det är mycket brandfarligt, tyngre än luft och har en narkotisk till kvävande effekt i höga koncentrationer.
Propan är extremt brandfarligt och bildar explosiva blandningar mellan 1,7 % och 10,8 volymprocent i luft. Dess antändningstemperatur är 470 °C (enligt DIN 51794). Värmevärdet är 12.874kWh/kg (butan 12.700kWh/kg).
Användning och tillverkning
Propan utvinns från naturgas eller produceras i ett petroleumraffinaderi när petroleum krackas.Det används i flytande form som bränsle och uppvärmningsgas (flytande gas), till exempel som autogas i bilar eller för varmluftsballonger, och som köldmedium (köldmediebeteckning R290) (se kylskåp), som en möjlig komponent av drivmedlet i sprayer och airsofts (butan används mest på grund av det lägre trycket), samt för produktion av eten och propen.
Lagring
Propan kondenseras under tryck och lagras i gasflaskor eller tankar.
Den förvaras också i underjordiska grottor. Lagring görs helst under de lågförbrukningsmånaderna för att kunna täcka förbrukningstoppar på vintern.
Reaktioner
Propan brinner och bildar koldioxid och vatten.
Referenser
- Geert Oldenburg:Propan – Butan . Springer (1955), ISBN B0000BM42L