Du kanske redan känner till bensoesyra som en kemikalie. Ja, denna ingrediens används ofta som en industriell mellanprodukt. Men har du hört talas om dess användning i mat? Hur görs det? Hur många av dess derivat? Varför är det mindre vanligt i mat än natriumbensoat? Vilka är vanliga användningsområden förutom i mat? …Du hittar alla dessa svar i den här artikeln (fortsätt läsa).
Bensoesyra (den europeiska livsmedelstillsatsen nummer E210), är en aromatisk karboxylsyra som inte vanligtvis används för konservering av livsmedel på grund av den svaga lösligheten i vatten. Det produceras vanligtvis till dess lösliga salter – ofta använda konserveringsmedel, natriumbensoat (E211) och kaliumbensoat (E212, inte vanligt, för att minska natriumintaget).
Naturlig källa
Bensoesyra kan finnas naturligt i fria eller kombinerade former i äpplen, tranbär, katrinplommon, plommon och så vidare.
Hur tillverkas bensoesyra?
Det finns två typer av bensoesyra, den ena är den naturliga formen som utvinns från växter och kan användas som smaksättning med FEMA nr. 2131. En annan är den mest använda, erhållen från toluensyntes och här skulle vi vilja introducera kort tillverkningsprocess av denna.
Toluenoxidation
Bensoesyra framställs till stor del kommersiellt genom vätskefasoxidation av toluen (från petrokemisk bearbetning) med syre i närvaro av en koboltkatalysator.
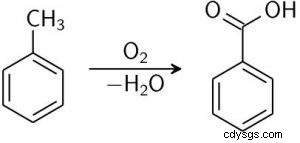
Om för livsmedel och farmaceutiska tillämpningar, måste andra tillverkningsprocesser (t.ex. sublimering, omkristallisation och neutralisering) utföras ytterligare för att rena rå bensoesyra eftersom den kan innehålla biprodukter såsom bensaldehyd, bensylalkohol och bensylbensoat. ()
Andra metoder
Bensoesyra av livsmedelskvalitet kan också tillverkas med följande två metoder som nämns av FDA ():
- smält ftalsyraanhydrid med en zinkoxidkatalysator
- hydrolys av bensotriklorid
Bensoesyra kan förresten även framställas av natriumbensoat med HCL.
Specifikation
| Andra namn |
|
| CAS-nummer | 65-85-0 |
| Kemisk formel | C7H6O2 eller C6H5COOH |
| Molarmassa | 122,123 g-mol-1 |
| Kokpunkt | 250 °C (482 °F; 523 K) |
| Smältpunkt | 122 °C (252 °F; 395 K) |
Egenskaper
- En vit kristallin flinga, nål, pulver eller granulat med lukt av bensoin eller bensaldehyd.
- Något lösligt i vatten medan lättlösligt i eter, etanol, diklormetan, dietyleter och andra organiska lösningsmedel.
- En svag syra och har en sur smak som påverkar smaken och pH-värdet på maten.
Struktur
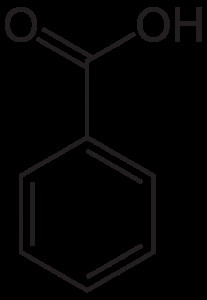
Strukturen är bensen med en karboxylsyra. Den är gjord av den funktionella gruppen karboxyl och aromatisk bensenring. Det kan finnas många derivat som genereras av reaktionerna mellan dessa två funktionella grupper och andra kemikalier.
1. Karboxylsyra
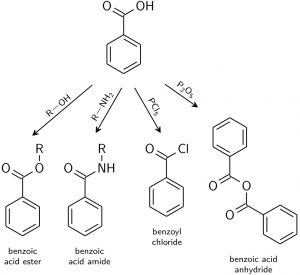
Karboxylsyra är lätt att reagera med andra grupper, såsom följande reaktioner:
- Tillverkning av natriumbensoat:med natriumbikarbonat eller natriumhydroxid.
- Förestring:med alkoholer för att bilda estrar, såsom metyl-, etyl-, butyl- eller hexylbensoat som används i artificiella smakämnen, dofter och personliga hygienprodukter. Eller genom reaktionen av två molekyler bensoesyra för att bilda bensoesyraanhydrid.
- Amideringsreaktion:med amino bildas bensoesyraamider.
- Ersättningsreaktion:OH i karboxylsyra kan ersättas med klorid för att erhålla bensoylklorid.
- Reduktion:bensylalkohol.
- Andra:som att göra bensaldehyd.
2. Aromatisk bensenring
Aromatisk bensenring kan även reagera med andra ämnen :
- Nitrering bildar m-nitrobensoesyra.
- Hydroxylering för att producera salicylsyra. Förresten, bensoesyra och salicylsyra kan användas tillsammans för att behandla hudirritation och inflammation.()
PKa
PKa för bensoesyra är 4,2. pKa-värdet används för att visa surheten eller styrkan hos en syra, eftersom svaga syror delvis dissocierar i vatten och når ett jämviktstillstånd.
Hur beräknar man PH för bensoesyralösning?
Bensoesyra är en svag syra och den dissocierar proton- och bensoatjoner efter dess reaktion med vatten.
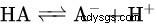
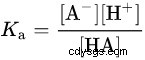
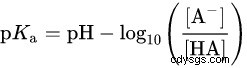
Ovan är dissociationsekvationen för bensoesyra och förhållandet mellan PKa och PH, HA står för bensoesyra, A- står för bensoatjon.
Steg 1:Antag att koncentrationen av totalt HA är 0,001 mol/L.
Det kan vara mer bensoesyralösligt än 0,001 mol/L om temperaturen är 25°C. För att vara exakt skulle molkoncentrationen vara n=löslighet/molekylformel, det vill säga n=3,44/122,123 =0,028mol/L. Här använder du 0,001 mol/L bara för att göra det enkelt.
Steg 2:Skriv joniseringsjämviktsekvationen enligt följande:
HA(aq)+H2O(l)⇌A−(aq)+H3O+(aq)
- [H3O+] är Hydroniumkoncentrationen
- [A−] är den konjugerade baskoncentrationen
- [HA] är bensoesyrakoncentrationen
Koncentrationen av [A−] och [H3O+] är densamma. Och vi antar att koncentrationen är X. Och slutkoncentrationen av HA i lösning är 0,001 – X.
Steg 3:Sedan kan ekvationen skrivas X*X/0,001-X =Ka.
Eftersom 0,001-X kan likna 0,001, så kan vi få X-värdet 10-3,6, så PH-värdet är 3,6.
Lätt polaritet och löslighet
Bensoesyra är strukturerad av en mindre polär karboxylsyragrupp fäst vid en stor, opolär bensenring. Eftersom den har en stor hydrofob bensenring anses den vara något polär.
I allmänhet kan polära föreningar lösas i polära lösningsmedel. Så det är därför bensoesyra är lätt löslig i vatten (polär) och löst i det opolära lösningsmedlet som eter och MTBE (metyl-tert-butyleter).
Även om etanol är polärt kan bensoesyra lösas upp i det eftersom båda kommer att ha en förestringsreaktion. Detta är ett undantag.
Lösligheten av bensoesyra i vatten eller i andra lösningsmedel relaterar i allmänhet till lösningsmedlens polära, lösningstemperaturen och andra lösningar, som NaOH eller HCl.
OK, låt oss se detaljerna enligt följande.
1. Vattenlöslighet
Bensoesyra är en svag syra, så den dissocierar endast delvis i vatten och är därför svagt löslig i vatten, med lösligheten 3,44 g/L i temperaturen 25 °C. Det kan lösas upp i varmt vatten eftersom den höga temperaturen främjar dissociationen till dess konjugerade basbensoatjon och med lösligheten 56,31 g/L i 100 °C.
2. Löslighet i NaOH
Bensoesyra är löslig i NaOH. Reaktionsmekanismen är följande:NaOH är en stark bas, den reagerar med den dissocierade protonen från bensoesyra och främjar sedan dissociationen av bensoesyra.
Det är så NaOH påverkar dess löslighet i vatten.
Och om det finns tillräckligt med NaOH kommer bensoesyra att dissocieras totalt och bilda natriumbensoat men förlorar sin konserverande aktivitet under alkaliska förhållanden.
3. Löslighet i HCl
I ett surt medium, som i HCl, blir bensoesyra mer olöslig. Eftersom ökningen av H+-joner kommer att göra dissociationsjämvikten till vänster, vilket gör den mer olöslig än i vatten.
HA(aq)+H2O(l)⇌A−(aq)+H3O+(aq)
Vad är användningen av bensoesyra?
Förutom dess tillämpning i livsmedel och drycker, kan bensoesyra även tillsättas till kosmetika och läkemedel för konservering. Dess huvudsakliga användning är dock som en prekursor för syntes av organiska kemikalier i olika industrier, såsom i parfymer, plaster, färgämnen och så vidare.
Som JECFA sa, för 30 år sedan var procentandelen och användningen av bensoesyra på marknaden följande ():
- 60 % användes för att producera fenol
- 30 % för kaprolaktam i nylonfibrer
- 5 % för produktion av natrium-, kalium- och kalciumbensoater
- 3 % för bensoylklorid
- 2 % för alkydhartser, bensoatestrar och andra
För närvarande förändras inte användningen mycket, bensoesyra används också som fodertillsats och som mellanprodukt i läkemedels- och plasttillverkning.
Låt oss titta närmare på dess olika användningsområden.
Mat
Bensoesyra av livsmedelskvalitet fungerar som ett konserveringsmedel som minskar tillväxten av mikroorganismer i sur mat. Det är mest aktivt på jästsvampar, och även på mögel och bakterier. Dess antimikrobiella aktivitet skulle vara bra vid pH-intervall från 2,5 till 4,0.
Varför är bensoesyra mindre vanligt i mat?
Men dess användningar i mat och dryck är inte vanliga jämfört med natriumbensoat och kaliumbensoat, som tre huvudfrågor (särskilt lösligheten):
- Löslighet:lätt löslig i vatten, inte lätt att använda
- PH:Det är en syra som påverkar PH-värdet i mat och dryck
- Smak:Dess lösning har en sur smak, påverkar smaken
Det är därför det alltid görs till sitt salt – natriumbensoat även om det är bensoesyra som har den antimikrobiella aktiviteten.
Typiska användningsnivåer av bensoesyra och natriumbensoat i livsmedel är mellan 0,05–0,1 %.
Följande mat kan innehålla det:
- Fruktjuice
- Pickles
- Sylt
- Mousserande drycker
- läsk
Kosmetika
Bensoesyra kan användas som bulkmedel, maskering och konserveringsmedel () i en mängd olika kosmetika och personliga vårdprodukter, inklusive:
- Hudvårdsprodukter:ansiktskräm, solkräm
- Munnvatten
Industriella mellanprodukter
Den industriella användningen är nära besläktad med den aromatiska ringen eller karboxylgruppen på den. Dess vanliga användningsområden är karboxylsyrareaktionen med andra ämnen, såsom för fenolproduktion, plast och bensylbensoat.
Fenol
Produktionen av fenol och kaprolaktam är den vanligaste användningen av bensoesyra.
Här är reaktionen:
C6H5CO2H + 1/2 O2 → C6H5OH + CO2
Fenol kan omvandlas till cyklohexanol, som kan användas i nylonsyntes. Fenoler kan också användas i hushållsrengöringsmedel och i munvatten som desinfektionsmedel.
Plast
Bensoesyra kan framställas till bensoatmjukgörare, såsom glykol-, dietylenglykol- och trietylenglykolestrar.
Är bensoesyra säker att äta?
Ja, dess livsmedelskvalitet har godkänts som en säker ingrediens av U.S. Food and Drug Administration (FDA), European Food Safety Authority (EFSA) samt Joint FAO/WHO Expert Committee on Food Additives (JECFA).
FDA
Bensoesyra anses allmänt vara säker (GRAS) som kan användas som ett antimikrobiellt medel, smakämne och adjuvans i livsmedel med en maximal användning av 0,1 %. Det kan också säkert användas i foder som konserveringsmedel eller surgörande medel. () ()
EFSA
Bensoesyra (E210) är listad i kommissionens förordning (EU) nr 231/2012 som en godkänd livsmedelstillsats och kategoriserad i "Andra tillsatser än färgämnen och sötningsmedel" ().
Säkerhetsutvärdering under 2016
Dess säkerhet omvärderades tillsammans med dess salter och EFSA härledde ett acceptabelt dagligt intag (ADI) på 5 mg/kg kroppsvikt per dag 2016.
Godkänd användning
Samma sak med natriumbensoat. ()
UK Food Standards Agency
Kategoriserad i "Andra" ()
Livsmedelsstandarder Australien Nya Zeeland
Det är en godkänd ingrediens i Australien och Nya Zeeland med kodnummer 210. ()
JECFA
Funktionsklass:livsmedelstillsatser, antimikrobiellt konserveringsmedel. ()
Acceptabelt dagligt intag:ADI “5 mg/kg kroppsvikt” fastställdes 1996 och ingen säkerhetsrisk som smakämne utvärderades 2002. ()
Vilka är möjliga biverkningar av bensoesyra?
När det kommer till biverkningarna av bensoesyra syftar det oftast på dess allergier och om den omvandlas till bensen som är cancerframkallande. Låt oss se detaljerna:
- Allergier:det kan orsaka irritationssymtom som hudutslag, rodnad eller till och med brännande känsla från ögon- och hudkontakt, och även vid inandning. ()
- Bensen:FDA nämner inte att bensoesyra bildas till bensen medan natrium- och kaliumbensoat gör det. ()
Är det säkert under graviditeten?
Bensoesyra anses allmänt vara säker för gravida, men det är bättre att rådgöra med din läkare för ditt användningstillstånd.
Slutsats
Nu kanske du har goda kunskaper om konserveringsmedlet – bensoesyra (E210), från följande aspekter:
- Naturlig källa
- Produktionsprocess
- Egenskaper
- Användningar
- Säkerhet
- Möjliga biverkningar
Om du har några frågor eller kommentarer om denna tillsats får du gärna meddela mig i kommentarerna.
