| wzór strukturalny | |||||||
|---|---|---|---|---|---|---|---|
| 2+ | |||||||
| Ogólne | |||||||
| Nazwa | węglan amonu | ||||||
| Inne nazwy | amon gazowany, sól jelonka | ||||||
| Formuła molekularna | (NH4 )2 CO3 | ||||||
| Numer CAS | 10361-29-2 | ||||||
| Krótki opis | bezbarwne ciało stałe | ||||||
| Właściwości | |||||||
| Masa molowa | 96,09 g mol | ||||||
| Stan materii | naprawiono | ||||||
| Gęstość | 1,6 g cm | ||||||
| Temperatura topnienia | rozkłada się w temperaturze 58 °C | ||||||
| Temperatura wrzenia | rozpada się przed | ||||||
| Ciśnienie pary | 0,69 Pa (20°C) | ||||||
| Rozpuszczalność | dobry w wodzie | ||||||
| Instrukcje bezpieczeństwa | |||||||
| |||||||
| Tam, gdzie jest to możliwe i powszechne, używane są jednostki SI. O ile nie zaznaczono inaczej, podane dane dotyczą standardowych warunków. | |||||||
Węglan amonu , (NH4 )2 CO3 H2 O, tworzy rozpuszczalne w wodzie, bezbarwne, sześcienne kryształy o masie cząsteczkowej Mr od 114.10. Rozkłada się całkowicie na amoniak, dwutlenek węgla i wodę w temperaturze 58 °C.
Właściwości
Sól tworzy bezbarwny proszek o słabym zapachu amoniaku. Ma gęstość około 1,6 g cm (w 20 °C) i wysoką rozpuszczalność w wodzie ok. 220 g/l. Roztwór reaguje słabo zasadowo, ustala się równowaga między amoniakiem NH3 , jony amonowe NH4 , jony węglanowe CO3 , jony wodorowęglanowe HCO3 i dwutlenek węgla CO2 a.
Sól reaguje zatem z wodą i kwasem węglowym, tworząc jony wodorowęglanowe i wodorotlenowe. Wodny roztwór węglanu amonu jest zatem stabilny tylko w obojętnym i słabo zasadowym środowisku - gazowy dwutlenek węgla ulatnia się w kwasach, a amoniak w stężonych alkaliach.
Synteza
Węglan amonu można wytworzyć w reakcji dwutlenku węgla z amoniakiem w roztworze wodnym.
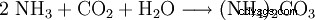
Innym sposobem wykazania tego jest ogrzewanie węglanu wapnia razem z siarczanem amonu.

W przypadku tej ostatniej metody wodorowęglan amonu i karbaminian amonu sublimują oprócz pożądanego węglanu amonu, pozostawiając siarczan wapnia w postaci stałej.
Wykorzystanie
Węglan amonu jest stosowany w syntezie heterocykli oraz jako dodatek w programach fotograficznych. Jest również stosowany w farbiarstwie, jako generator dwutlenku węgla w gaśnicach oraz jako sól zapachowa.
Jest również używany jako środek spulchniający (znany również jako sól staghorn).W UE jest oznaczony jako E 503i jako dodatek do żywności zatwierdzone.
Węglan amonu jest często używany w chemii nieorganicznej do analizy jakościowej w celu wytrącenia kationów baru, strontu i wapnia metali ziem alkalicznych z nieznanej próbki jako grupy, oddzielenia ich i zidentyfikowania za pomocą reakcji wykrywania.

