Vous connaissez peut-être déjà l'acide benzoïque en tant que produit chimique. Oui, cet ingrédient est couramment utilisé comme intermédiaire industriel. Mais avez-vous entendu parler de ses utilisations dans l'alimentation ? Comment est-ce fait? Combien de ses dérivés ? Pourquoi est-il moins courant dans les aliments que le benzoate de sodium ? Quelles sont les utilisations courantes en dehors de la nourriture ? …Vous trouverez toutes ces réponses dans cet article (continuez à lire).
L'acide benzoïque (numéro d'additif alimentaire européen E210) est un acide carboxylique aromatique qui n'est pas couramment utilisé pour la conservation des aliments en raison de sa légère solubilité dans l'eau. Il est généralement produit à ses sels solubles - conservateurs largement utilisés, benzoate de sodium (E211) et benzoate de potassium (E212, peu courant, pour réduire l'apport en sodium).
Source naturelle
L'acide benzoïque peut être naturellement présent sous forme libre ou combinée dans les pommes, les canneberges, les pruneaux, les prunes, etc.
Comment l'acide benzoïque est-il fabriqué ?
Il existe deux types d'acide benzoïque, l'un est la forme naturelle extraite des plantes et peut être utilisé comme arôme avec le FEMA n ° 2131. Un autre est le plus utilisé, obtenu à partir de la synthèse du toluène et ici nous aimerions présenter le bref processus de fabrication de celui-ci.
Oxydation du toluène
L'acide benzoïque est en grande partie produit commercialement par oxydation en phase liquide du toluène (provenant du traitement pétrochimique) avec de l'oxygène en présence d'un catalyseur au cobalt.
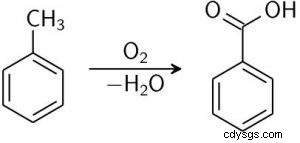
Si pour des applications alimentaires et pharmaceutiques, d'autres procédés de fabrication (par exemple, la sublimation, la recristallisation et la neutralisation) doivent être exécutés davantage pour purifier l'acide benzoïque brut car il peut contenir des sous-produits tels que le benzaldéhyde, l'alcool benzylique et le benzoate de benzyle. ()
Autres méthodes
L'acide benzoïque de qualité alimentaire peut également être fabriqué à partir des deux méthodes suivantes mentionnées par la FDA ():
- anhydride phtalique fondu avec un catalyseur d'oxyde de zinc
- hydrolyse du trichlorure de benzo
Soit dit en passant, l'acide benzoïque peut également être produit à partir de benzoate de sodium avec HCL.
Spécification
| Autres noms |
|
| Numéro CAS | 65-85-0 |
| Formule chimique | C7H6O2 ou C6H5COOH |
| Masse molaire | 122.123 g·mol−1 |
| Point d'ébullition | 250 °C (482 °F ; 523 K) |
| Point de fusion | 122 °C (252 °F ; 395 K) |
Propriétés
- Un flocon cristallin blanc, une aiguille, une poudre ou un granulé avec une odeur de benjoin ou de benzaldéhyde.
- Légèrement soluble dans l'eau, mais facilement soluble dans l'éther, l'éthanol, le dichlorométhane, l'éther diéthylique et d'autres solvants organiques.
- Un acide faible et un goût acide qui influencera le goût et le PH des aliments.
Structure
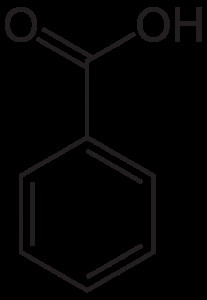
La structure est le benzène avec un acide carboxylique. Il est composé du groupe fonctionnel carboxyle et du cycle benzénique aromatique. De nombreux dérivés peuvent être générés par les réactions de ces deux groupes fonctionnels avec d'autres produits chimiques.
1. Acide carboxylique
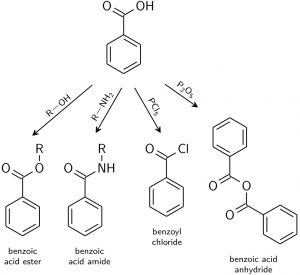
L'acide carboxylique est facile à réagir avec d'autres groupes, comme les réactions suivantes :
- Produire du benzoate de sodium :avec du bicarbonate de sodium ou de l'hydroxyde de sodium.
- Estérification :avec des alcools pour former des esters, tels que le benzoate de méthyle, d'éthyle, de butyle ou d'hexyle utilisé dans les arômes artificiels, les parfums et les produits de soins personnels. Ou par la réaction de deux molécules d'acide benzoïque pour former de l'anhydride d'acide benzoïque.
- Réaction d'amidation :avec des formes aminées d'amides d'acide benzoïque.
- Réaction de remplacement :OH dans carboxylique peut être remplacé par du chlorure pour obtenir du chlorure de benzoyle.
- Réduction :alcool benzylique.
- Autres :comme pour fabriquer du benzaldéhyde.
2. Anneau de benzène aromatique
Le noyau benzénique aromatique peut également réagir avec d'autres substances :
- La nitration forme de l'acide m-nitrobenzoïque.
- Hydroxylation pour produire de l'acide salicylique. Soit dit en passant, l'acide benzoïque et l'acide salicylique peuvent être utilisés ensemble pour traiter l'irritation et l'inflammation de la peau.()
PKa
Le PKa de l'acide benzoïque est de 4,2. La valeur pKa est utilisée pour montrer l'acidité ou la force d'un acide, car les acides faibles se dissocient partiellement dans l'eau et atteignent un état d'équilibre.
Comment calculer le PH d'une solution d'acide benzoïque ?
L'acide benzoïque est un acide faible et il dissocie les ions proton et benzoate après sa réaction avec l'eau.
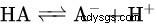
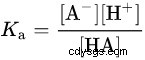
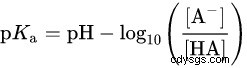
Ci-dessus se trouve l'équation de dissociation de l'acide benzoïque et la relation entre PKa et PH, HA signifie acide benzoïque, A- signifie ion benzoate.
Étape 1 :Supposons que la concentration de HA total est de 0,001 mol/L.
Il peut y avoir plus d'acide benzoïque soluble que 0,001 mol/L si à la température de 25°C. Pour être exact, la concentration molaire serait n=solubilité/formule moléculaire, c'est-à-dire n=3,44/122,123 =0,028mol/L. Ici, nous utilisons 0,001 mol/L juste pour simplifier les choses.
Étape 2 :Écrivez l'équation d'équilibre d'ionisation comme suit :
HA(aq)+H2O(l)⇌A−(aq)+H3O+(aq)
- [H3O+] est la concentration d'hydronium
- [A−] est la concentration en base conjuguée
- [HA] est la concentration en acide benzoïque
La concentration de [A−] et [H3O+] est la même. Et nous supposons que la concentration est X. Et la concentration finale de HA en solution est de 0,001 - X.
Étape 3 :Ensuite, l'équation peut s'écrire X*X/0,001-X =Ka.
Comme 0,001-X peut être similaire à 0,001, nous pouvons donc obtenir la valeur X 10-3,6, donc la valeur PH est 3,6.
Légèrement polarité et solubilité
L'acide benzoïque est structuré par un groupe acide carboxylique polaire plus petit attaché à un gros cycle benzénique non polaire. Comme il possède un grand cycle benzénique hydrophobe, il est considéré comme légèrement polaire.
Généralement, les composés polaires peuvent se dissoudre dans des solvants polaires. C'est pourquoi l'acide benzoïque est légèrement soluble dans l'eau (polaire) et dissous dans le solvant non polaire comme l'éther et le MTBE (méthyl tert-butyl éther).
Bien que l'éthanol soit polaire, l'acide benzoïque peut s'y dissoudre car les deux auront une réaction d'estérification. Ceci est une exception.
La solubilité de l'acide benzoïque dans l'eau ou dans d'autres solvants est généralement liée à la polaire des solvants, à la température de la solution et à d'autres solutions, comme NaOH ou HCl.
OK, voyons les détails comme suit.
1. Solubilité dans l'eau
L'acide benzoïque est un acide faible, il ne se dissocie donc que partiellement dans l'eau et est donc légèrement soluble dans l'eau, avec une solubilité de 3,44 g/L à une température de 25 °C. Il peut se dissoudre dans l'eau chaude car la température élevée favorise la dissociation en son ion benzoate de base conjugué, et avec une solubilité de 56,31 g/L à 100 °C.
2. Solubilité dans NaOH
L'acide benzoïque est soluble dans NaOH. Le mécanisme réactionnel est le suivant :NaOH est une base forte, il réagit avec le proton dissocié de l'acide benzoïque et favorise alors la dissociation de l'acide benzoïque.
C'est ainsi que NaOH affecte sa solubilité dans l'eau.
Et s'il y a suffisamment de NaOH, l'acide benzoïque sera totalement dissocié et formera du benzoate de sodium mais perd son activité conservatrice dans des conditions alcalines.
3. Solubilité dans HCl
Dans un milieu acide, comme dans HCl, l'acide benzoïque devient plus insoluble. Comme l'augmentation des ions H+ rendra l'équilibre de dissociation vers la gauche, le rendant plus insoluble que dans l'eau.
HA(aq)+H2O(l)⇌A−(aq)+H3O+(aq)
Quelles sont les utilisations de l'acide benzoïque ?
Outre son application dans les aliments et les boissons, l'acide benzoïque peut également être ajouté aux cosmétiques et aux produits pharmaceutiques pour la conservation. Cependant, son utilisation principale est comme précurseur pour la synthèse de produits chimiques organiques dans diverses industries, telles que les parfums, les plastiques, les colorants, etc.
Comme l'a dit le JECFA, il y a 30 ans, les pourcentages et les utilisations de l'acide benzoïque sur le marché étaient les suivants ():
- 60 % ont été utilisés pour produire du phénol
- 30 % pour le caprolactame dans les fibres de nylon
- 5 % pour la production de benzoates de sodium, de potassium et de calcium
- 3 % pour le chlorure de benzoyle
- 2 % pour les résines alkydes, les esters de benzoate et autres
Actuellement, les utilisations ne changent pas beaucoup, l'acide benzoïque est également utilisé comme additif alimentaire et comme intermédiaire dans la fabrication de produits pharmaceutiques et de plastiques.
Voyons de plus près ses différentes utilisations.
Nourriture
L'acide benzoïque de qualité alimentaire fonctionne comme un conservateur qui diminue la croissance des micro-organismes dans les aliments acides. Il est surtout actif sur les levures, mais aussi sur les moisissures et les bactéries. Son activité antimicrobienne serait bonne dans les gammes de pH de 2,5 à 4,0.
Pourquoi l'acide benzoïque est moins courant dans les aliments ?
Mais ses utilisations dans les aliments et les boissons ne sont pas courantes par rapport au benzoate de sodium et au benzoate de potassium, car trois problèmes principaux (en particulier la solubilité) :
- Solubilité :légèrement soluble dans l'eau, pas facile à utiliser
- PH :C'est un acide qui va influencer le PH des aliments et des boissons
- Goût :sa solution a un goût acide, affectera le goût
C'est pourquoi il est toujours fabriqué à son sel - le benzoate de sodium bien que ce soit l'acide benzoïque qui ait l'activité antimicrobienne.
Les niveaux d'utilisation typiques de l'acide benzoïque et du benzoate de sodium dans les aliments se situent entre 0,05 et 0,1 %.
Les aliments suivants peuvent en contenir :
- Jus de fruits
- Cornichons
- Confitures
- Boissons pétillantes
- Soda
Cosmétiques
L'acide benzoïque peut être utilisé comme gonflant, masquant et conservateur () dans une variété de produits cosmétiques et de soins personnels, notamment :
- Produits de soin :crème hydratante pour le visage, crème solaire
- Bains de bouche
Intermédiaires industriels
L'utilisation industrielle est étroitement liée au cycle aromatique ou au groupe carboxyle qu'il contient. Ses utilisations courantes sont la réaction de l'acide carboxylique avec d'autres substances, telles que la production de phénol, les plastiques et le benzoate de benzyle.
Phénol
La production de phénol et de caprolactame est l'utilisation la plus courante de l'acide benzoïque.
Voici la réaction :
C6H5CO2H + 1/2 O2 → C6H5OH + CO2
Le phénol peut être converti en cyclohexanol, qui peut être utilisé dans la synthèse du nylon. Les phénols peuvent également être utilisés dans les nettoyants ménagers et dans les bains de bouche comme désinfectant.
Plastiques
L'acide benzoïque peut être transformé en benzoate de plastifiants, tels que les esters de glycol, de diéthylèneglycol et de triéthylèneglycol.
L'acide benzoïque peut-il être consommé sans danger ?
Oui, sa qualité alimentaire a été approuvée comme ingrédient sûr par la Food and Drug Administration (FDA) des États-Unis, l'Autorité européenne de sécurité des aliments (EFSA), ainsi que par le Comité mixte FAO/OMS d'experts sur les additifs alimentaires (JECFA).
FDA
L'acide benzoïque est généralement reconnu comme sûr (GRAS) et peut être utilisé comme agent antimicrobien, agent aromatisant et adjuvant dans les aliments avec une utilisation maximale de 0,1 %. Il peut également être utilisé en toute sécurité dans les aliments pour animaux comme agent de conservation ou acidifiant. () ()
EFSA
L'acide benzoïque (E210) est répertorié dans le règlement (UE) n° 231/2012 de la Commission en tant qu'additif alimentaire autorisé et classé dans la catégorie "Additifs autres que les colorants et les édulcorants" ().
Réévaluation de la sécurité en 2016
Sa sécurité a été réévaluée avec ses sels et l'EFSA a calculé une dose journalière admissible (DJA) de 5 mg/kg pc par jour en 2016.
Utilisations approuvées
Idem avec celui du benzoate de sodium. ()
Agence britannique des normes alimentaires
Classé dans "Autres" ()
Normes alimentaires Australie Nouvelle-Zélande
C'est un ingrédient approuvé en Australie et en Nouvelle-Zélande avec le numéro de code 210. ()
JECFA
Classe de fonction :additifs alimentaires, conservateur antimicrobien. ()
Dose journalière acceptable :DJA "5 mg/kg pc" établie en 1996 et aucun problème de sécurité en tant qu'agent aromatisant évalué en 2002. ()
Quels sont les effets secondaires possibles de l'acide benzoïque ?
En ce qui concerne les effets secondaires de l'acide benzoïque, il s'agit généralement de ses allergies et de sa conversion en benzène, qui est cancérigène. Voyons les détails :
- Allergies :il peut provoquer des symptômes d'irritation tels que des éruptions cutanées, des rougeurs ou même une sensation de brûlure au contact des yeux et de la peau, ainsi que par inhalation. ()
- Benzène :la FDA ne mentionne pas que l'acide benzoïque forme du benzène, contrairement au benzoate de sodium et de potassium. ()
Est-ce sans danger pendant la grossesse ?
L'acide benzoïque est généralement considéré comme sûr pour les femmes enceintes, mais il est préférable de consulter votre médecin pour votre condition d'utilisation.
Conclusion
Maintenant, vous avez peut-être une bonne connaissance du conservateur – acide benzoïque (E210), sous les aspects suivants :
- Source naturelle
- Processus de fabrication
- Propriétés
- Utilisations
- Sécurité
- Effets secondaires possibles
Si vous avez des questions ou des remarques sur cet additif, n'hésitez pas à me le faire savoir dans les commentaires.
