Patrice Cani (UCLouvain) i Claude Knauf (INSERM) odkryli „zagłuszacz”, który blokuje komunikację między jelitami a mózgiem, zapobiegając w ten sposób prawidłowej regulacji cukru i powodując insulinooporność u osób z cukrzycą. Odkryli również, że lipid wytwarzany przez nasz organizm pomaga zapobiegać tej dysfunkcji i regulować poziom cukru, łagodząc w ten sposób cukrzycę i stany zapalne jelit. Odkrycia te, opublikowane w czasopiśmie naukowym GUT, są ważne, ponieważ obecnie co drugi Europejczyk ma nadwagę, a co dziesiąty ma cukrzycę. Źródło:UCLouvain
Od 2004 roku Claude Knauf (INSERM) i Patrice Cani (Université Catholique de Louvain) współpracują nad mechanizmami molekularnymi i komórkowymi, aby zrozumieć przyczyny rozwoju cukrzycy typu 2, a przede wszystkim zidentyfikować nowe cele terapeutyczne. W 2013 r. stworzyli międzynarodowe laboratorium „NeuroMicrobiota Lab” (INSERM-UCLouvain), aby zidentyfikować powiązania między mózgiem a bakteriami jelitowymi.
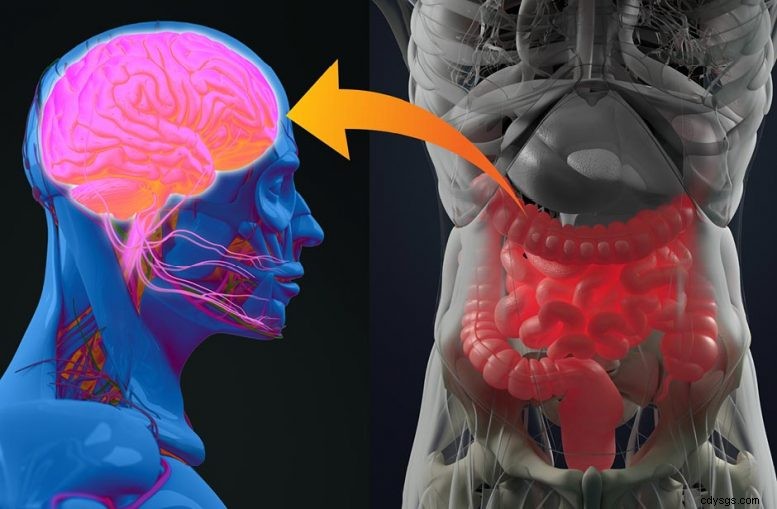
Bardzo szybko zrozumieli, że oś jelita-mózg odgrywa główną rolę w regulacji poziomu cukru we krwi. Kiedy jemy, jelito (zwane również „drugim mózgiem” ze względu na tworzące je neurony) kurczy się i trawi pokarm. Cukier i tłuszcz dostają się do organizmu, a ich poziom wzrasta we krwi. Wykorzystując ten cukier i tłuszcz, organizm wykonuje swoją pracę lub je przechowuje. U osoby z cukrzycą ten proces przebiega nieprawidłowo, a poziom cukru wzrasta w nieprawidłowych proporcjach.
Idąc krok dalej, obaj badacze zaobserwowali, że jelita podczas trawienia wysyłają sygnał do mózgu, aby dowiedzieć się, co zrobić z przychodzącymi tłuszczami i cukrami. Mózg wysyła wiadomość do różnych narządów (wątroby, mięśni, tkanki tłuszczowej), aby przygotować się do obniżenia poziomu cukru i tłuszczu we krwi. Jednak u osoby z cukrzycą ten mechanizm nie działa. Naukowcy zaobserwowali, że jelita działają nieprawidłowo i nie wysyłają sygnału do mózgu. Przyczyną jest nadmierna kurczliwość jelit, która zakłóca komunikację z mózgiem. Nagle komendy usunięcia cukru z krwi przestają mijać. Cukier pozostaje, powodując hiperglikemię. Mechanizm wpływa również na działanie insuliny:brak komunikatu oznacza brak działania insuliny, co skutkuje insulinoopornością.
Naukowcy starali się zrozumieć tę nadmierną kurczliwość, obserwując różnice w budowie jelita, a także działanie prebiotyków w mikrobiocie u myszy „normalnych” i „cukrzycowych”. Zaobserwowali, że u myszy z cukrzycą, ale także u osób z cukrzycą, występuje poważny niedobór określonego lipidu (chociaż jest on naturalnie obecny w jelitach zdrowych pacjentów). Zespół przetestował zatem wpływ lipidów na wykorzystanie cukrów, na skurcz jelit i ostatecznie na cukrzycę. Członkowie zespołu badawczego NeuroMicrobiota, Anne Abot i Eve Wemelle, odkryli, że lipid jest kluczem do przywrócenia wykorzystania cukru. Działa bezpośrednio na drugi mózg.
Dzisiaj zespół odkrył i zrozumiał, w jaki sposób nasze bakterie jelitowe (lub mikrobiota jelitowa) odgrywają ważną rolę w zmianie produkcji bioaktywnych lipidów, a stamtąd w przywracaniu doskonałej komunikacji między jelitami a mózgiem. Stąd niektóre z tych lipidów są niezbędnymi przekaźnikami, które działają na bardzo precyzyjne cele w drugim mózgu (enkefaliny lub receptory opioidowe). Możliwości leczenia obejmują modyfikację produkcji takich lipidów przez organizm, mogą lub przyjmowanie ich doustnie. Te ścieżki są obecnie badane.
Stosując to samo podejście, zespół badawczy INSERM-UCLouvain przyczynił się do odkrycia nowego bioaktywnego lipidu, który zmniejsza stan zapalny jelit. Jest bezpośrednio wytwarzany przez pewne bakterie jelitowe, również zidentyfikowane w tym badaniu, dlatego te dwa podejścia, lipid lub jedna lub więcej bakterii, mogą służyć jako cel terapeutyczny.
Według WHO co trzeci ze 150 000 ludzi, którzy umierają każdego dnia, jest ofiarą chorób układu krążenia. Połowa populacji Belgii ma nadwagę i stwarza ryzyko chorób układu krążenia i cukrzycy typu 2. Te badania UCLouvain i INSERM mogą potencjalnie mieć wpływ na dużą część populacji.
Odniesienie:„Identyfikacja nowych enterosyn przy użyciu prebiotyków:rola bioaktywnych lipidów i sygnalizacji receptora opioidowego mi u ludzi i myszy” Anne Abot, Eve Wemelle, Claire Laurens, Adrien Paquot, Nicolas Pomie, Deborah Carper, Arnaud Bessac, Xavier Mas Orea , Christophe Fremez, Maxime Fontanie, Alexandre Lucas, Jean Lesage, Amandine Everard, Etienne Meunier, Gilles Dietrich, Giulio G Muccioli, Cedric Moro, Patrice D Cani i Claude Knauf, 5 października 2020 r., Gut .
DOI:10.1136/gutjnl-2019-320230
Aby przeprowadzić te badania, Patrice Cani z UCLouvain otrzymał fundusze z kilku źródeł, w tym WELBIO, FNRS i Baillet-Latour Fund.
