| wzór strukturalny | |||||||
|---|---|---|---|---|---|---|---|
| 2 Na | |||||||
| Ogólne | |||||||
| Nazwa | Siarczan sodu | ||||||
| Inne nazwy | siarczan disodowy, E 514, sól Glaubera (Na2 SO4 · 10 godz.2 O) | ||||||
| Formuła molekularna | Na2 SO4 | ||||||
| Numer CAS | 7757-82-6 | ||||||
| Krótki opis | bezbarwne i bezwonne kryształy | ||||||
| Właściwości | |||||||
| Masa molowa | 142,04 g mol | ||||||
| Stan materii | naprawiono | ||||||
| Gęstość | 2,70 g cm | ||||||
| Temperatura topnienia | 884°C | ||||||
| Temperatura wrzenia | 1689°C | ||||||
| Rozpuszczalność | dobra w wodzie:170 g/l, w 20 °C | ||||||
| Instrukcje bezpieczeństwa | |||||||
| |||||||
| Tam, gdzie jest to możliwe i powszechne, używane są jednostki SI. O ile nie zaznaczono inaczej, podane dane dotyczą standardowych warunków. | |||||||
Siarczan sodu (Na2 SO4 , przestarzała nazwa Siarczan sodu ) jest solą sodową kwasu siarkowego i składa się z dwóch kationów Na (Na) i anionu siarczanowego (SO4 ) razem. Dekahydrat (Na2 SO4 · 10 godz.2 O) jest również nazywany Glaubersalz na cześć chemika Johanna Rudolpha Glaubera Nazywany także solą Carlsbad , który jest otrzymywany przez odparowanie wody mineralnej Karlowe Wary, składa się głównie z dekahydratu siarczanu sodu i jest używany jako środek przeczyszczający, podobnie jak sól Glaubera.
Historia
Siarczan sodu został wyprodukowany i opisany około 1655 roku przez chemika i farmaceutę Johanna Rudolpha Glaubera. Sam nazwał odkrytą sól Sal mirabilis i Mirabili .
Uzyskiwanie i wyświetlanie
Siarczan sodu jest rzadko wydobywany z naturalnych minerałów, ponieważ często jest produktem ubocznym reakcji przemysłu chemicznego, w których kwas siarkowy jest neutralizowany sodą kaustyczną. Inną możliwością przedstawienia technicznego jest reakcja soli kamiennej (NaCl) z kwasem siarkowym w celu uzyskania kwasu solnego z siarczanem sodu jako produktem ubocznym (w 800°C):
-
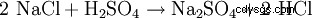
- Chlorek sodu i kwas siarkowy reagują, tworząc siarczan sodu i chlorowodór.
Siarczan sodu można wytworzyć w laboratorium w następujących reakcjach:
-

- Sód i kwas siarkowy reagują, tworząc siarczan sodu i wodór.
-
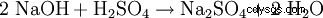
- Siarczan sodu i woda powstają podczas neutralizacji sody kaustycznej kwasem siarkowym.
Właściwości
Bezwodny siarczan sodu topi się w 884°C, jest higroskopijny i łatwo rozpuszczalny w wodzie po podgrzaniu (ciepło rozpuszczania). Natomiast dekahydrat rozpuszcza się przy silnym chłodzeniu, ze względu na tzw. efekt entropii. Dekahydrat siarczanu sodu jest składnikiem wielu wód mineralnych i powoli topi się we własnej wodzie krystalicznej od około 32°C. Bezwodna sól oddziela się od tego roztworu, który jest przesycony bezwodnym siarczanem sodu.
Wykorzystanie
Siarczan sodu jest stosowany w detergentach jako wypełniacz, w medycynie jako środek przeczyszczający, w produkcji pulpy (proces siarczanowy) oraz w przemyśle szklarskim, tekstylnym i farbiarskim. Wyżarzony, bezwodny siarczan sodu jest używany w laboratorium do suszenia rozpuszczalników organicznych. Dekahydrat siarczanu sodu (sól Glaubera ) jest używany jako środek przeczyszczający i magazynujący ciepło utajone.
W technologii spożywczej jest stosowany jako środek ujędrniający, regulator kwasowości i nośnik.Siarczan sodu i wodorosiarczan sodu są dodatkami do żywności oznaczonymi w UE E 514 bez maksymalnego limitu (satysfakcja kwantowa ) ogólnie zatwierdzone do żywności.
Źródła
- ↑ https://www.zusatzstoffe-online.de/zusatzstoffe/216.e514_natriumsulfate.html
