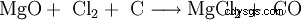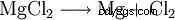| fórmula estructural | |||||||
|---|---|---|---|---|---|---|---|
| No hay fórmula estructural disponible | |||||||
| General | |||||||
| Nombre | Cloruro de Magnesio | ||||||
| Otros nombres | E511 | ||||||
| Fórmula molecular | MgCl2 | ||||||
| Número CAS | 7786-30-3 (anhidro) 7791-18-6 (hexahidrato) | ||||||
| Breve descripción | cristales blancos | ||||||
| Propiedades | |||||||
| Masa molar | 95,21 g mol | ||||||
| Estado de la materia | arreglado | ||||||
| Densidad | 2,32 g·cm | ||||||
| Punto de fusión | 708 °C | ||||||
| Punto de ebullición | 1412 °C | ||||||
| Presión de vapor | 0,1 mbar (650 °C) | ||||||
| Solubilidad | 542 g/L (20 °C) | ||||||
| Instrucciones de seguridad | |||||||
| |||||||
| MAC | 20 mg·m | ||||||
| Donde sea posible y común, se utilizan unidades SI. A menos que se indique lo contrario, los datos proporcionados se aplican en condiciones estándar. | |||||||
Cloruro de magnesio , MgCl2 , es la sal de magnesio del ácido clorhídrico. Forma varios hidratos.
Ocurrencias
El cloruro de magnesio se encuentra naturalmente en el mineral carnalita (KMgCl3 · 6H2 0) como una sal doble. Otra fuente natural es el agua de mar. Allí es la sal más común después del cloruro de sodio.
Obtención y visualización
La extracción técnica del cloruro de magnesio se realiza por evaporación de los licores finales de la producción de cloruro de potasio. Primero, el cloruro de magnesio hexahidratado (MgCl2 · 6H2 O) recibido. La evaporación adicional produce un producto con un contenido de agua más bajo. El cloruro de magnesio anhidro se obtiene haciendo reaccionar óxido de magnesio con coque y cloro:
En el laboratorio, el cloruro de magnesio se puede hacer a partir de hidróxido de magnesio y ácido clorhídrico
o haciendo reaccionar magnesio con ácido clorhídrico
ser ganado.
Propiedades
El cloruro de magnesio es altamente higroscópico. Su tendencia a la hidrólisis es menos pronunciada que la del cloruro de aluminio (AlCl3 ). El cloruro de magnesio anhidro cristaliza en CdCl2 -tipo de rejilla.
El cloruro de magnesio hexahidratado (número CAS:7791−18−6) tiene una masa molar de 203,3 g mol, una densidad de 1,57 g cm y un punto de fusión de aproximadamente 117 °C (descomposición). La solubilidad del hexahidrato es de 1700 g/L (a 20 °C).
Uso
El cloruro de magnesio se utiliza para obtener magnesio elemental mediante electrólisis de sales fundidas:
Se utiliza junto con el óxido de magnesio en cemento para soleras, como sal para carreteras y como aditivo alimentario con la etiqueta (número E) E 511. Sirve como potenciador del sabor artificial y está aprobado para alimentos orgánicos.
Además, el cloruro de magnesio se utiliza para aumentar la concentración de magnesio en los acuarios de arrecife.
Fuentes
- ↑ Base de datos de sustancias peligrosas de BGIA Gestis