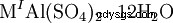| strukturformel | |||||||
|---|---|---|---|---|---|---|---|
| 2 Al 3 | |||||||
| Allmänt | |||||||
| Namn | Aluminiumsulfat | ||||||
| Andra namn | Svavelhaltig aluminiumoxid | ||||||
| Molekylformel | Al2 (SO4 )3 | ||||||
| CAS-nummer | 10043-01-3 | ||||||
| Kort beskrivning | vitt pulver | ||||||
| Egenskaper | |||||||
| Molarmassa | 342,15 g/mol | ||||||
| Sakens tillstånd | fixat | ||||||
| Densitet | 2,71 g/cm | ||||||
| Smältpunkt | 770 °C (sönderdelning) | ||||||
| Kokpunkt | - | ||||||
| Ångtryck | - (-) | ||||||
| Löslighet | bra i vatten | ||||||
| Säkerhetsinstruktioner | |||||||
| |||||||
| MAK | 6 mg/m (Al) | ||||||
| Där det är möjligt och vanligt används SI-enheter. Om inget annat anges gäller de angivna uppgifterna under standardvillkor. | |||||||
Aluminiumsulfat , molekylformel Al2 (SO4 )3 , bildar ett färglöst pulver med en rel. Molekylmassa Mr på 342,15 och en densitet på 2,71 g/cm.
Förekomster
I naturen förekommer aluminiumsulfat till exempel i alun.
Syntes
Hydratet av aluminiumsulfat kan erhållas genom att lösa ren aluminiumoxid i konc. Skaffa svavelsyra.
Lyhördhet
Med en sur reaktion löses aluminiumsulfat i vatten och kristalliseras som monoklinisk Al2 vid rumstemperatur (SO4 )3 · 18H2 O ut. Från en temperatur på 340 °C är saltet helt uttorkat och över 770 °C bryts det ner till aluminiumoxid och svaveltrioxid
Aluminiumsulfat bildar dubbelsalter med sulfaterna av envärda metaller enligt följande formel (alun):
Användning
- Hjälpanställd inom pappersindustrin
- Flockningsmedel vid behandling av dricksvatten
- Beredningsmedel i färgverk och som fröberedning
- Komponent av släckskum
- Som isolerande salt (på färska cement- eller kalkstenssubstrat, mot vatten- och nikotinfläckar) vid renoveringar
- Ingrediens av växtförstärkare och skyddsmedel
- Det tillsätts i livsmedel som ett uppstramande eller stabiliseringsmedel. Det finns i EU som livsmedelstillsats med beteckningen E 520 godkänd.
Källor
- ↑ Materialsäkerhetsdatablad (alfa-aesar)
- ↑ BGIA Gestis databas för farliga ämnen
- ↑ BVL