| wzór strukturalny | |||||||
|---|---|---|---|---|---|---|---|
| Ogólne | |||||||
| Nazwa | Mocznik | ||||||
| Inne nazwy |
| ||||||
| Formuła molekularna | CH4 N2 O | ||||||
| Numer CAS | 57-13-6 | ||||||
| Krótki opis | bezbarwne, krystaliczne ciało stałe o zapachu przypominającym amoniak | ||||||
| Właściwości | |||||||
| Masa molowa | 60,06 g mol | ||||||
| Stan materii | naprawiono | ||||||
| Gęstość | 1.3230g cm | ||||||
| Temperatura topnienia | 132,5-134,5°C | ||||||
| Temperatura wrzenia | Rozkład od 130 °C | ||||||
| Ciśnienie pary | 0,2 Pa (75°C) | ||||||
| Rozpuszczalność | łatwo rozpuszczalny w wodzie:ok. 1000 g l (20 °C), rozpuszczalny w etanolu:50 g l (20 °C), słabo rozpuszczalny w eterze i chloroformie | ||||||
| Instrukcje bezpieczeństwa | |||||||
| |||||||
| WGK | 1 | ||||||
| Tam, gdzie jest to możliwe i powszechne, używane są jednostki SI. O ile nie zaznaczono inaczej, podane dane dotyczą standardowych warunków. | |||||||
Mocznik (łac. mocznik), znany również jako diamid kwasu węglowego – nie mylić z kwasem moczowym – jest związkiem organicznym, który jest wytwarzany przez wiele zwierząt jako końcowy produkt metabolizmu związków azotowych (np. aminokwasów) w tzw. cyklu mocznikowego i wydalane z moczem. Czysty mocznik to białe, krystaliczne, nietoksyczne i higieniczne ciało stałe o słabym zapachu amoniaku.
Historia
Mocznik był pierwszym syntetycznie wytworzonym związkiem organicznym. Został odkryty jako substancja przez Hilaire Rouelle w 1773 roku i po raz pierwszy zsyntetyzowany sztucznie przez Friedricha Wöhlera w 1828 roku w reakcji cyjanianu potasu i siarczanu amonu. Było to sprzeczne z rozpowszechnionym wówczas poglądem, że substancje organiczne można znaleźć w istotach żywych w zasadzie tylko poprzez tak zwane "vis vitalis". (siła życiowa) może zostać wytworzona i utorować drogę chemii organicznej.
Znaczenie fizjologiczne
Mocznik pochodzi z metabolizmu białek i aminokwasów i należy do substancji moczowych, aby zapobiec tworzeniu się amoniaku (NH3 ) z grup aminowych są one w trakcie cyklu mocznikowego przenoszone do nietoksycznej cząsteczki mocznika w wątrobie, która jest wydalana jako końcowy produkt metaboliczny przez nerki.
Choroby, takie jak ostra lub przewlekła niewydolność nerek i zaburzenia czynności nerek związane z cukrzycą, mogą prowadzić do podwyższonych wartości mocznika w surowicy/osoczu.
Zaburzenia i osobliwości: Wysokie spożycie białka prowadzi do zwiększonych wartości mocznika nawet przy prawidłowej czynności nerek, co czyni go słabym parametrem nerek.
Aplikacje
Ze względu na wysoką zawartość azotu wynoszącą 46% mocznik jest najważniejszym nawozem azotowym na świecie. Ze względu na wysoką zdolność wiązania wody mocznik jest również często stosowany jako czynnik nawilżający w kosmetykach. W farmacji mocznik jest znany jako środek keratolityczny. Ta właściwość jest używana w różnych przepisach. Na przykład jest wysoce skoncentrowany (40%) w pastach wraz ze środkiem przeciwgrzybiczym (środek przeciwgrzybiczy) przeciwko grzybicy paznokci (grzybica paznokci), dzięki czemu mocznik zmiękcza paznokieć, dzięki czemu zakażoną substancję paznokcia można usunąć kawałek po kawałku. Jest również stosowany jako środek nawilżający w maściach do zwalczania egzemy atopowej i chorób porostów.
Producenci papierosów dodają mocznik do tytoniu, dzięki czemu nikotyna może być lepiej przyswajalna poprzez zwiększenie wartości pH. W ten sposób rzekomo lekkie papierosy o niskiej zawartości nikotyny na paczce stają się mocnymi papierosami.
Mocznik może być również stosowany jako zamiennik soli drogowej; jednak ze względu na koszty nie jest to opłacalne.
W technologii silników wysokoprężnych mocznik jest wtryskiwany za filtrem sadzy do gorącego strumienia spalin, aby zredukować tlenki azotu w spalinach. Zużycie wynosi około 2 do 8% w stosunku do paliwa.
Jest dodawany do żywności jako stabilizator. W UE jest wymieniony jako dodatek do żywności z oznaczeniem E 927b Dopuszczony wyłącznie do gumy do żucia bez dodatku cukru.
Właściwości
Gdy się topi, mocznik rozkłada się z uwolnieniem amoniaku (NH3 ) do Biureta:
Produkcja przemysłowa
Mocznik jest produkowany przemysłowo w dużych ilościach (2004:127 mln t na całym świecie) i jest używany m.in. B. jako nawóz azotowy lub jako NOx -Reduktor w procesie SNCR. W krajach o dużych złożach gazu ziemnego, który kiedyś był po prostu spalany, obecnie gaz ziemny przekształcany jest w mocznik. Do tego celu wykorzystywane są duże instalacje, które finalnie produkują mocznik z gazu ziemnego, powietrza i wody w etapach procesowych produkcja wodoru → produkcja amoniaku → synteza mocznika. CO2 związane jako mocznik i nie uwalniane do atmosfery. Mocznik, który jest początkowo w roztworze, jest przekształcany w granulki i sprzedawany w workach lub luzem. Największe zakłady na świecie produkują około 4000 ton mocznika dziennie.
Równania reakcji:
-
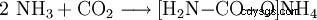
- Amoniak i dwutlenek węgla reagują, tworząc karbaminian amonu.
-
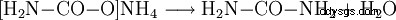
- Karbaminian amonu reaguje, tworząc mocznik i wodę.
Przemysłowym dalszym zastosowaniem mocznika jest produkcja melaminy, która jest wykorzystywana m.in. B. jest przetwarzany z formaldehydem na żywice syntetyczne, oraz żywice mocznikowo-formaldehydowe (żywice mocznikowe, tzw. UF), z. B. używane do produkcji płyt wiórowych.
Źródła
- ↑ Baza danych substancji BGIA GESTIS:https://www.hvbg.de/d/bia/gestis/stoffdb/index.html . 23 lipca 2007
- AdBlue
- Azotan mocznika
- tiomocznik
