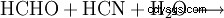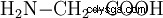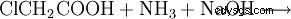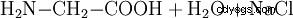| formula strutturale | ||
|---|---|---|
| Generale | ||
| nome | Glicina | |
| Abbreviazione | Gly, G | |
| Restname | glicile | |
| essenziale | no | |
| Altri nomi | Glicole, Glicole, Acido Aminoacetico | |
| Formula molecolare | C2 H5 NO2 | |
| Numero CAS | 56-40-6 | |
| Breve descrizione | solido bianco | |
| Proprietà | ||
| Massa molare | 75,07 g/mol | |
| Stato della materia | risolto | |
| Densità | 1.595 g/cm | |
| Punto di fusione | 450-500°F | |
| Punto di ebollizione | > 230 °C di decomposizione termica | |
| Pressione di vapore | Pa (°C) | |
| catena laterale | nessuna catena laterale, altrimenti idrofila | |
| Solubilità | buono in acqua (225 g/l a 20 °C), povero in alcool, insolubile in solventi apolari | |
| punto isoelettrico | 6.06 | |
| valori pK a 25 °C | pKCOOH :2,4 pKNH2 :9.8 | |
| volume di van der Waals | 48 | |
| Valutazione dell'idrofobicità | -0,4 | |
| Istruzioni di sicurezza | ||
| ||
| Frasi R e S | R:nessuna frase di rischio S:nessuna frase S | |
| MAC | non impostato | |
| Ove possibile e comune, vengono utilizzate le unità SI. Salvo diversa indicazione, i dati forniti si applicano a condizioni standard. | ||
Glicina (Chimicamente chiamato acido aminoacetico), è l'amminoacido proteinogenico più piccolo e semplice. Appartiene al gruppo degli aminoacidi idrofili ed è l'unico amminoacido proteinogenico che non è chirale e quindi non otticamente attivo.
La glicina non è essenziale, quindi può essere prodotta dall'organismo umano stesso ed è un componente importante di quasi tutte le proteine e un nodo importante nel metabolismo.
Il nome deriva dal sapore dolce della glicina pura (gr. glycis :Dolce).
Sintesi
La glicina si forma, tra l'altro, nella reazione di formaldeide, acido cianidrico e acqua:
Questa reazione è di particolare importanza per l'ipotesi che i materiali di partenza potrebbero essersi formati dalla cosiddetta atmosfera primordiale che circondava la terra circa 4 miliardi di anni fa. Aveva un presumibilmente fatto di idrogeno (H2 ), elio (He) e in misura minore metano (CH4 ), ammoniaca (NH3 ) e alcuni altri gas nobili.
Chimicamente, la glicina può anche essere preparata da acido monocloroacetico e ammoniaca:
Nel corpo, la maggior parte della glicina si ottiene dal cibo, ma può anche essere prodotta dalla serina.
Funzioni
Metabolismo
La conversione della serina in glicina, oltre a produrre glicina, serve anche a convertire l'acido tetraidrofolico in acido N-N-metilene-tetraidrofolico, necessario, tra l'altro, per la sintesi dei nucleotidi di timina (componente del DNA).
La glicina è necessaria anche direttamente per la sintesi di altri componenti del materiale genetico (purina). Serve anche alla biosintesi dell'eme (legatura dell'ossigeno nel sangue), della creatina (accumulo di energia nei muscoli) o del glutatione.
Come cosiddetto aminoacido glucogenico, la glicina può essere convertita in glucosio tramite il piruvato come parte del metabolismo.
L'acido ossalico tossico può anche essere formato dalla glicina come sottoprodotto.
È particolarmente comune nel collagene, la proteina più comune negli organismi animali. Qui rappresenta un buon terzo di tutti gli amminoacidi, poiché le sue piccole dimensioni consentono al collagene di avvolgersi nella sua struttura a tripla elica.
sistema nervoso
La glicina agisce nel sistema nervoso centrale attraverso il recettore della glicina come neurotrasmettitore inibitorio, cioè come sostanza di segnalazione inibitoria. Agisce aprendo i canali del cloro ligando-dipendenti, portando a un potenziale postsinaptico inibitorio (IPSP), che riduce l'attività dei neuroni a valle.
Le cellule nervose a rilascio di glicina (neuroni glicinergici) si trovano principalmente nel midollo spinale e inibiscono i cosiddetti motoneuroni del corno anteriore, determinando una riduzione dell'attività muscolare dei muscoli innervati dalle cellule.
La stricnina, un antagonista del recettore della glicina, e la tossina tetanica, che inibisce il rilascio di glicina, causano una riduzione dell'effetto della glicina. La perdita dell'inibizione aumenta l'attività muscolare. Questo può portare a crampi potenzialmente letali.
Utilizzo
La glicina viene aggiunta agli alimenti come esaltatore di sapidità.
La glicina e il suo sale di sodio sono numerati E 640 come additivo alimentare nell'UE Generalmente approvato per alimenti senza limiti di quantità massima, gli effetti sulla salute non sono noti.
Riferimenti
- G. Löffler, P. E. Petrides:Biochimica e patobiochimica , 7a edizione, Springer Verlag, 2003, ISBN 3-540-42295-1