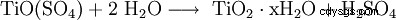| formula strutturale | |||||||
|---|---|---|---|---|---|---|---|
| Nessuna formula strutturale disponibile | |||||||
| Generale | |||||||
| Nome | ossido di titanio (IV) | ||||||
| Altri nomi |
| ||||||
| Formula molecolare | O2 Ti | ||||||
| Numero CAS | 13463-67-7 | ||||||
| Breve descrizione | polvere cristallina bianca | ||||||
| Proprietà | |||||||
| Massa molare | 79,90 g mol | ||||||
| Stato della materia | risolto | ||||||
| Densità | 4,24 g cm | ||||||
| Punto di fusione | 1855°C | ||||||
| Punto di ebollizione | 2900°C | ||||||
| Solubilità | cattivo in acido fluoridrico, acido nitrico e solforico concentrato, insolubile in acqua, acido cloridrico, acido nitrico e solforico diluito | ||||||
| Istruzioni di sicurezza | |||||||
| |||||||
| Proprietà termodinamiche | |||||||
| ΔHf | −249 kJ/mol (rutilo) | ||||||
| Ove possibile e comune, vengono utilizzate le unità SI. Salvo diversa indicazione, i dati forniti si applicano a condizioni standard. | |||||||
ossido di titanio (IV) (Biossido di titanio ) è uno degli ossidi di titanio.
Occorrenze
L'ossido di titanio (IV) si trova naturalmente in tre modifiche:
- Il rutilo è un minerale tetragonale di portamento prevalentemente prismatico. Il nome rutilo deriva dal latino rutilus – rossastro. Il rutilo ha una densità di 4,26 g/cm. È particolarmente popolare come pigmento bianco.
- L'anatasio forma cristalli oloedrici tetragonali (oloedrico significa il gruppo più simmetrico all'interno di un sistema cristallino, nel tetragonale quindi 4/m 2/m 2/m). L'anatasio gradualmente (più rapidamente da una temperatura di oltre 700 °C) si trasforma irreversibilmente in rutilo. La densità dell'anatasio è 3,88 g/cm. L'anatasio funge anche da pigmento bianco.
- La brookite forma minerali ortorombici e non funge da pigmento bianco. La brookite si trasforma anche in rutilo al di sotto del punto di fusione.
Poiché i depositi naturali hanno colori inquietanti che z. B. dal ferro in ilmenite (FeTiO3 ) sono causati, questi vengono raffinati nel processo al solfato o al processo con cloruro (preferito).
Ottenere e visualizzare
Per solvolisi (idrolisi) del composto Ti(IV):
Proprietà
Il punto di fusione del biossido di titanio è 1855 °C. È termicamente stabile, durevole, ha un alto indice di rifrazione (2,8) e quindi un ottimo potere colorante e coprente. Il biossido di titanio è chimicamente molto inerte. È resistente alla luce, poco costoso, completamente atossico e quindi il pigmento bianco più importante.
Utilizzo
Il biossido di titanio è usato come colorante bianco. Fu scoperto in Norvegia e negli Stati Uniti nel 1908 e lì prodotto dal 1909 con il nome di Kronos Titanium White. La produzione iniziò in Germania nel 1924 con il nome di Degea-Titanweiß. Il bianco di titanio è stato prodotto solo nella forma anatasio fino al 1938, ma poi principalmente nella forma rutilo, che si è rivelata più stabile ai leganti dell'olio e ai coloranti organici. Per questo veniva anche chiamato bianco rutilo.
Il bianco titanio ha la più alta opacità di tutti i pigmenti bianchi e un'ottima capacità schiarente. È chimicamente stabile, non tossico e si trova con la denominazione E 171 come additivo alimentare, ad esempio, nel dentifricio e nelle gocce per la tosse. A volte è anche usato nella pittura a olio. In campo tecnico trova impiego nelle pitture e vernici (ad es. per pitture murali e tessili), nella carta e come bloccante UV nelle creme solari e schiarenti nei medicinali (compresse). L'effetto fotocatalitico di TiO2 Le nanoparticelle sono utilizzate in connessione con l'attività UV per le superfici "autopulenti" (autopulizia fotocatalitica). La cella solare colorante (cella di Grätzel) si basa ancora sulle proprietà dei semiconduttori del biossido di titanio. Il biossido di titanio è anche utilizzato come componente principale del dielettrico ceramico nei condensatori ceramici di Classe 1.
Il biossido di titanio nella modifica dell'anatasio è il componente principale dei catalizzatori utilizzati per la denitrificazione industriale dei gas di combustione mediante il processo SCR.
La produzione di ossido di titanio mediante il processo al solfato produce acido diluito (acido solforico diluito), parte del quale viene riutilizzato per la produzione di ossido di titanio mediante concentrazione. In alcuni paesi, parte di questo acido diluito viene ancora scaricato nei fiumi e nei mari o scaricato, mentre il processo del cloruro non produce acido diluito. Il cloro utilizzato rimane in gran parte nel ciclo di processo.
TiO2 trova impiego anche nel campo della finitura delle piastrelle, il che significa che le superfici delle piastrelle trattate diventano repellenti allo sporco.
Prova
Il biossido di titanio appena precipitato al freddo è anfotero e solubile in acidi minerali diluiti. La digestione avviene con solfato di idrogeno di potassio in un crogiolo di porcellana. Si scioglie quindi in acqua fredda con poco acido solforico. Con poche gocce di perossido di idrogeno, il giallo (base) al giallo-arancio (acido, foto) [Ti(O2 ) aq] catione Acido cloridrico e zinco (granuli) formano idrogeno nascente, che trasforma Ti(IV) in rosso-viola [Ti(H2 O)6 ] ridotto.
Nanotecnologie
Prove individuali
- ↑ Voce sull'ossido di titanio(IV) nel database delle sostanze GESTIS della BGIA, recuperato il 29 novembre 2007 (JavaScript richiesto)
- ↑ Susanne Donner:Pulire con il potere della luce . Technology Review, n. 7, luglio 2006, pp. 19 e segg.