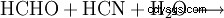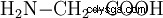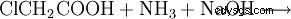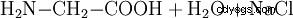| formule structurelle | ||
|---|---|---|
| Général | ||
| nom | Glycine | |
| Abréviation | Gly, G | |
| Nom de repos | glycyle | |
| essentiel | non | |
| Autres noms | Glycol, glycol, acide aminoacétique | |
| Formule moléculaire | C2 H5 NON2 | |
| Numéro CAS | 56-40-6 | |
| Brève description | solide blanc | |
| Propriétés | ||
| Masse molaire | 75,07 g/mol | |
| État de la matière | corrigé | |
| Densité | 1,595 g/cm | |
| Point de fusion | 450-500 °F | |
| Point d'ébullition | > Décomposition thermique à 230 °C | |
| Pression de vapeur | Pa (°C) | |
| chaîne latérale | pas de chaîne latérale, sinon hydrophile | |
| Solubilité | bon dans l'eau (225 g/l à 20 °C), pauvre en alcool, insoluble dans les solvants apolaires | |
| point isoélectrique | 6.06 | |
| Valeurs pK à 25 °C | pKCOOH :2,4 pKNH2 :9.8 | |
| tome van der Waals | 48 | |
| Évaluation de l'hydrophobicité | -0.4 | |
| Consignes de sécurité | ||
| ||
| Phrases R et S | R :pas de phrases de risque S :pas de phrases S | |
| MAK | non défini | |
| Lorsque cela est possible et courant, les unités SI sont utilisées. Sauf mention contraire, les données indiquées s'appliquent dans des conditions standard. | ||
Glycine (chimiquement appelé acide aminoacétique), est le plus petit et le plus simple des acides aminés protéinogènes. Il appartient au groupe des acides aminés hydrophiles et est le seul acide aminé protéinogène non chiral et donc non optiquement actif.
La glycine n'est pas essentielle, elle peut donc être produite par l'organisme humain lui-même et est un composant important de presque toutes les protéines et un nœud important du métabolisme.
Le nom dérive du goût sucré de la glycine pure (gr. glycis :Sucré).
Synthèse
La glycine se forme, entre autres, lors de la réaction du formaldéhyde, du cyanure d'hydrogène et de l'eau :
Cette réaction revêt une importance particulière en raison de l'hypothèse selon laquelle les matières premières auraient pu se former à partir de l'atmosphère dite primordiale qui entourait la terre il y a environ 4 milliards d'années. Elle avait vraisemblablement un composé d'hydrogène (H2 ), de l'hélium (He) et dans une moindre mesure du méthane (CH4 ), ammoniac (NH3 ) et quelques autres gaz nobles.
Chimiquement, la glycine peut aussi être préparée à partir d'acide monochloroacétique et d'ammoniac :
Dans le corps, la plus grande partie de la glycine provient des aliments, mais elle peut également être fabriquée à partir de la sérine.
Fonctions
Métabolisme
En plus de produire de la glycine, la conversion de la sérine en glycine sert également à convertir l'acide tétrahydrofolique en acide N-N-méthylène-tétrahydrofolique, nécessaire, entre autres, à la synthèse des nucléotides de la thymine (composant de l'ADN).
La glycine est également requise directement pour la synthèse d'autres composants du matériel génétique (purines). Il sert également à la biosynthèse de l'hème (liaison de l'oxygène dans le sang), de la créatine (stockage d'énergie dans les muscles) ou du glutathion.
En tant qu'acide aminé dit glucogénique, la glycine peut être convertie en glucose via le pyruvate dans le cadre du métabolisme.
De l'acide oxalique toxique peut également se former à partir de la glycine en tant que sous-produit.
Il est particulièrement courant dans le collagène, la protéine la plus courante dans les organismes animaux. Ici, il représente un bon tiers de tous les acides aminés, car sa petite taille permet au collagène de s'enrouler dans sa structure en triple hélice.
système nerveux
La glycine agit dans le système nerveux central via le récepteur de la glycine en tant que neurotransmetteur inhibiteur, c'est-à-dire en tant que substance de signalisation inhibitrice. Il agit en ouvrant des canaux chlorure ligand-dépendants, conduisant à un potentiel post-synaptique inhibiteur (IPSP), qui réduit l'activité des neurones en aval.
Les cellules nerveuses libérant de la glycine (neurones glycinergiques) se trouvent principalement dans la moelle épinière et inhibent les soi-disant motoneurones de la corne antérieure, entraînant une réduction de l'activité musculaire des muscles innervés par les cellules.
La strychnine, un antagoniste du récepteur de la glycine, et la toxine tétanique, qui inhibe la libération de la glycine, entraînent une diminution de l'effet de la glycine. La perte d'inhibition augmente l'activité musculaire. Cela peut entraîner des crampes potentiellement mortelles.
Utilisation
La glycine est ajoutée aux aliments comme exhausteur de goût.
La glycine et son sel de sodium portent le numéro E 640 en tant qu'additif alimentaire dans l'UE Généralement approuvé pour les aliments sans restriction de quantité maximale, les effets sur la santé ne sont pas connus.
Références
- G. Löffler, P. E. Petrides :Biochimie et pathobiochimie , 7e édition, Springer Verlag, 2003, ISBN 3-540-42295-1