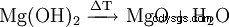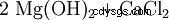| wzór strukturalny | |||||||
|---|---|---|---|---|---|---|---|
| Brak dostępnej formuły strukturalnej | |||||||
| Ogólne | |||||||
| Nazwa | Wodorotlenek magnezu | ||||||
| Inne nazwy | Wodorotlenek magnezu(II), brucyt, E528 | ||||||
| Formuła molekularna | Mg(OH)2 | ||||||
| Numer CAS | 1309-42-8 | ||||||
| Krótki opis | biały proszek | ||||||
| Właściwości | |||||||
| Masa molowa | 58,33 g mol | ||||||
| Stan materii | naprawiono | ||||||
| Gęstość | 2,38 g cm | ||||||
| Temperatura topnienia | Rozkład 350 °C | ||||||
| Rozpuszczalność | nie w wodzie i alkoholu, dobra w roztworach soli amonowych i rozcieńczonych kwasach (L=1 10 mol l; w wodzie o temp. 25°C) | ||||||
| Instrukcje bezpieczeństwa | |||||||
| |||||||
| MAK | nie ustawiono | ||||||
| Tam, gdzie jest to możliwe i powszechne, używane są jednostki SI. O ile nie zaznaczono inaczej, podane dane dotyczą standardowych warunków. | |||||||
Wodorotlenek magnezu Mg(OH)2 jest amorficznym białym proszkiem. W naturze występuje sporadycznie jako brucyt mineralny. Sieć krystaliczna brucytu składa się z sześciokątnego, najbliższego upakowania kuli jonów wodorotlenowych. Co druga warstwa szczeliny oktaedrycznej jest zajęta przez jony magnezu (Mg).
Właściwości
Wodorotlenek magnezu jest słabo rozpuszczalny w wodzie i roztworach zasadowych, ale łatwo rozpuszczalny w roztworach kwaśnych (np. kwas solny, kwas azotowy). Wodorotlenek magnezu jest również łatwo rozpuszczalny w roztworach soli amonowych, ponieważ jony wodorotlenkowe są przechwytywane przez jony amonowe:
-
 .
.
Wodorotlenek magnezu tworzy z kwasami sole zasadowe i obojętne.
W temperaturach powyżej 350 °C następuje powolny rozkład do tlenku magnezu. W temperaturze 600 °C równowaga jest praktycznie po stronie tlenkowej.
Uzyskiwanie i wyświetlanie
Wodorotlenek magnezu można otrzymać z pozostałości po ekstrakcji potażu przez wytrącanie mlekiem wapiennym (1) lub z wody morskiej przez wytrącanie palonym dolomitem (2). Produkt jest następnie filtrowany i suszony w około 100°C. Szczególnie czysty wodorotlenek magnezu powstaje w wyniku działania wody na pierwiastkowy magnez (3).
(1) 
(2) 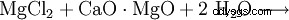
(3) 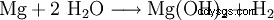
Wykorzystanie
Większość wodorotlenku magnezu produkowanego do celów przemysłowych jest dalej przetwarzana na tlenek magnezu przez kalcynację (wypalanie) w temperaturze 500–600 °C.
Wodorotlenek magnezu jest stosowany jako dodatek do oleju jadalnego (do wiązania dwutlenku siarki), jako flokulant do oczyszczania ścieków, jako środek zmniejszający palność w tworzywach termoplastycznych (poliolefiny, PVC) i elastomerach oraz jako dodatek do detergentów.
W medycynie jest stosowany jako środek zobojętniający kwas (lek neutralizujący kwas żołądkowy) i jako bardzo silny środek przeczyszczający.
Wodorotlenek magnezu jest dodawany do żywności jako regulator kwasowości lub środek antyadhezyjny. Jest zatwierdzony w UE jako dodatek do żywności pod numerem E E 528.
Źródła
- ↑ Baza danych substancji niebezpiecznych BGIA Gestis