| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
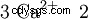 | |||||||
| Allgemeines | |||||||
| Nazwa | Cytrynian wapnia | ||||||
| Kolejne imię |
| ||||||
| Wzór sumy | C12 H10 Ca3 O14 | ||||||
| Numer CAS | 813-94-5 (wasserfrei) 5785-44-4 (tetrahydrat) | ||||||
| Zmiana schematu | weißer, geruchloser, kristalliner Feststoff | ||||||
| Właściwości własne | |||||||
| Masa molowa | 570,5 g·mol (tetrahydrat) | ||||||
| Zagregowanie | festiwal | ||||||
| Schmelzpunkt | Zersetzungstemperatur (Tetrahydrat): 120 °C Poch.> | ||||||
| Zamknij | gering löslich w Wasser:1 g·l (25 °C); unlöslich w etanolu; leicht löslich in verdünnten Säuren | ||||||
| Sicherheitshinweise | |||||||
| |||||||
| WGK | 1 | ||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||
Cytryt wapnia (di-[2-hydroksy-1,2,3-propantrikarboksylat]-tetrahydrat triwapnia) , ein Salz der Citronensäure, ist ein weißer, geruchloser, geschmacksneutraler, kristalliner Feststoff.
Gewinnung und Darstellung
Die Herstellung erfolgt durch Neutralization von Citronensäure mittels einer Calciumquelle wie Calciumhydrooxid. Bei dieser exothermen Fällungsreaktion werden pro Teil Calciumcitrat vier Moleküle Wasser („Kristallwasser”) gebunden.
-

- Calciumhydroxid und Citronensäure reagieren zu Tricalciumdicitrat und Wasser.
Właściwości własne
Der Calciumgehalt beträgt 21 %. Die Wasserlöslichkeit steigt mit sinkender Temperatura (odwrotna Löslichkeit) und sinkendem pH-Wert. Aufgrund der organischen Citronensäure und der damit verbundenen höheren Löslichkeit ist die Bioverfügbarkeit des enthaltenen Calciums höher als bei den anorganischen Calciumsalzen wie Calciumcarbonat, Calciumphosphat.
Rozszerzenie
Neben dem lange bekannten positiven Einfluss von Calcium auf die Knochendichte (s. Osteoporose), zeigen neuere Untersuchungen, dass bei einer ausreichenden Calciumzufuhr auch das Risiko für Übergewicht und Fettibigkeit Aus diesen Gründen wird Calciumcitrat Nahrungsmitteln zur Calciumanreicherung zugesetzt und für Nahrungsergänzungsmittel (Żywność funkcjonalna) verwendet. Es wird aber auch als Säureregulator und Stabilisator und in Arznei-, Futter- und Zahnpflegemitteln eingesetzt.Es ist in der EU als Lebensmittelzusatzstoff der Nummer E 333 zugelassen.
Quellen
- ↑ de.chemdat.info
Literatura i linki do stron internetowych
- Römpp Chemielexikon, 9. Aufl. (Herausgeber:Falbe/Regitz), S. 553
- Kurt Schreier, Hans Wolf:Untersuchungen über den Einfluß der Citronensäure auf den Calciumstoffwechsel. European Journal of Pediatrics, tom. 67, nr 5 (1950) 526-544
- HJ Heller, LG Greer, SD Haynes, Poindexter JR i CY Pak:Porównanie farmakokinetyczne i farmakodynamiczne dwóch suplementów wapnia u kobiet po menopauzie. Journal of Clinical Pharmacology, tom. 40 (2000) 1237–1244
- Davies KM, Heaney RP, Recker RR i in.:Spożycie wapnia i masa ciała. Journal of Clinical Endocrinology &Metabolism, tom. 85, nr 12 (2000) 4635-4638
- Heaney RP, Davies KM, Barger-Lux MJ:Wapń i waga:badania kliniczne. Journal of the American College of Nutrition, tom. 21, nr 2 (2002) 152S–155S
- Parikh SJ, Yanovski JA:Spożycie wapnia i otyłość. American Journal of Clinical Nutrition, tom. 77, nr 2 (2003) 281–287
- Pereira MA, Jacobs DR, Jr., Van Horn L, Slattery ML, Kartashov AI, Ludwig DS:Spożycie nabiału, otyłość i zespół oporności na insulinę u młodych dorosłych:badanie CARDIA. Jama, tom. 287, nr 16 (2002) 2081-2089
- Zemel MB, Shi H, Greer B, Dirienzo D, Zemel PC:Regulacja otyłości przez wapń w diecie. Dziennik Faseb, tom. 14 (2000) 1132-1138
