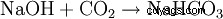Lessive de soude est le nom des solutions d'hydroxyde de sodium (NaOH) dans l'eau. Ces solutions sont des solutions alcalines.
L'hydroxyde de sodium se dissout très bien dans l'eau, générant beaucoup de chaleur. Une solution aqueuse saturée à température ambiante contient 1260 g d'hydroxyde de sodium par litre. La soude caustique est l'un des produits chimiques de laboratoire et industriels les plus couramment utilisés. La soude caustique concentrée est très corrosive pour la peau et même la soude caustique fortement diluée peut endommager la cornée des yeux à un point tel qu'elle peut entraîner la cécité.
Une molaire de soude caustique (une solution contenant une mole de NaOH (40 g) dans un litre; équivalant à environ 3,9 % en poids) a un pH de 14.
La force de base est pKb =−2,43.
| Teneur massique NaOH (wt%) | 4.0 | 10.0 | 20.0 | 30.0 | 40.0 | 50.0 |
|---|---|---|---|---|---|---|
| Molarité NaOH (mol/l) | 1.04 | 2.77 | 6.09 | 9.95 | 14h30 | 19.05 |
| Concentration NaOH (g/l) | 41,7 | 110.9 | 243.8 | 398.3 | 572.0 | 762.2 |
| Densité de la solution (g/cm) | 1 043 | 1 109 | 1 219 | 1 328 | 1 430 | 1 524 |
Extraction
La soude caustique est généralement obtenue à partir de chlorure de sodium par électrolyse (environ 65 % de la production mondiale). Du chlore est également produit dans le processus. Les grands besoins de l'industrie chimique en soude caustique ont largement contribué au développement de la chimie du chlore (exemple :chlorure de polyvinyle comme utilisation complémentaire du chlore).
Utilisation
- Nettoyage :rinçage des bouteilles dans les usines d'embouteillage de boissons (brasseries et autres entreprises de transformation de boissons), nettoyage des canalisations, élimination des salissures grasses et huileuses
- Fabrication de savons, digestion de la bauxite (pour l'extraction de l'aluminium) et d'autres minerais, production de pâte
- Transformation :décapage du bois, épluchage à grande échelle (par exemple des pommes de terre), neutralisation des acides, régénération du caoutchouc et des échangeurs d'ions, transformation du coton (mercerisation)
- utilisation ultérieure en photographie, pour la conservation de documents anciens
- Développer des circuits imprimés exposés pour la production de circuits imprimés, qui ont été préalablement recouverts d'un vernis spécial (photo-positif).
- Production de bretzels (par exemple, bretzels ou bâtonnets de bretzels)
- Sans vidange (Une cuillère à soupe de NaOH avec une tasse d'eau tiède dans le drain d'un évier bouché, par exemple)
- Clivage des doubles brins d'ADN en simples brins en cassant les liaisons hydrogène entre les bases nucléotidiques complémentaires.
Stockage
La soude caustique ne doit jamais être stockée dans des récipients avec des bouchons en verre rodé. Du bicarbonate de sodium se forme sur la coupe avec le dioxyde de carbone de l'air.
Cette croûte de sel colle le rodage au boîtier. Au lieu de cela, un récipient en plastique en z. B. PE-HD avec bouchon à vis ou bouchon en caoutchouc.
Élimination
Étant donné que la soude caustique elle-même est très souvent utilisée pour lier d'autres produits chimiques très dangereux pour l'environnement, il n'y a rien de mal à rejeter de la soude caustique non contaminée dans le système d'égout sous une forme suffisamment diluée, à condition que les eaux usées soient envoyées vers une station d'épuration.