| struttura cristallina | |||||||
|---|---|---|---|---|---|---|---|
| Nessuna formula strutturale disponibile | |||||||
| Generale | |||||||
| Nome | Ossido di magnesio | ||||||
| Altri nomi | Magnesia | ||||||
| Formula del rapporto | MgO | ||||||
| Numero CAS | 1309-48-4 | ||||||
| Breve descrizione | cristalli incolori | ||||||
| Proprietà | |||||||
| Massa molare | 40 g/mol | ||||||
| Stato della materia | risolto | ||||||
| Densità | 3,65 g cm | ||||||
| Punto di fusione | ~2800 °C | ||||||
| Punto di ebollizione | ~3600 °C | ||||||
| Solubilità | praticamente insolubile in acqua | ||||||
| Istruzioni di sicurezza | |||||||
| |||||||
| Ove possibile e comune, vengono utilizzate le unità SI. Salvo diversa indicazione, i dati forniti si applicano a condizioni standard. | |||||||
Ossido di magnesio (MgO ) o Magnesia è un sale costituito da ioni Mg e O. Cristallizza nel reticolo del cloruro di sodio. L'ossido di magnesio è prodotto bruciando magnesio, può essere ottenuto per precipitazione dall'acqua di mare o può essere prodotto riscaldando un composto di magnesio (ad esempio idrossido di magnesio Mg(OH)2 ). o carbonato di magnesio MgCO3 ).
In quest'ultimo caso, il comportamento chimico dell'ossido di magnesio dipende molto dalla temperatura di produzione e dal processo produttivo. Quando il carbonato di magnesio naturale (magnesite) viene "bruciato" a circa 800 °C, viene prodotta la cosiddetta "magnesite caustica bruciata". L'anidride carbonica fuoriesce durante il processo di cottura, ma la temperatura è troppo bassa per consentire la sinterizzazione. I grani di ossido di magnesio risultanti hanno quindi ancora la forma esterna di carbonato di magnesio, sono porosi e molto reattivi a causa dell'ampia superficie interna. Con l'acqua si forma in breve tempo idrossido di magnesio. La reazione di alcuni sali di magnesio disciolti in acqua con la magnesite caustica bruciata porta alla cristallizzazione di un ammasso duro come una roccia. È il sale di magnesio cloruro di magnesio MgCl2 , si parla di cemento Sorel. Viene utilizzato per la produzione di pavimenti industriali. Inoltre, la magnesite caustica bruciata viene utilizzata nell'industria dei fertilizzanti e dei mangimi come supporto di magnesio. L'ossido di magnesio viene utilizzato anche per la terapia sostitutiva.
A una temperatura compresa tra 1700 ° C e 2000 ° C si forma magnesia sinterizzata, sopra 2800 ° C magnesia fusa. Entrambe le varietà difficilmente reagiscono con l'acqua. La magnesia sinterizzata viene utilizzata per i rivestimenti dei forni e per le apparecchiature di laboratorio a causa della sua resistenza al fuoco (punto di fusione 2800 °C). La magnesia è utilizzata nella produzione di refrattari di base per la produzione di cemento, estrazione di metalli non ferrosi, raffinerie di acciaio e vetro, e nella fabbricazione di mattoni di magnesia-carbonio, il materiale principale utilizzato nella fabbricazione di rivestimenti refrattari per navi siderurgiche (convertitore, forno elettrico ad arco e siviera). Senza magnesia, questi materiali non possono essere fabbricati con metodi moderni. Questo materiale veniva utilizzato in passato anche per isolare i tubi tra il filamento e il catodo dei tubi elettronici a causa della sua resistenza al calore.
L'ossido di magnesio si trova naturalmente come minerale vulcanico periclasi prima. Sono cristalli da grigio a verde scuro, vetrosi e regolari con una durezza da 5,5 a 6.
Viene aggiunto agli alimenti come regolatore di acidità o agente antiagglomerante ed è classificato come additivo alimentare E 530 nell'UE senza limite massimo (quantum satis ) generalmente approvato per gli alimenti.
Produzione
Esistono diversi modi per produrre ossido di magnesio:
Il vapore di etanolo (se riscaldato) reagisce con il magnesio per formare ossido di magnesio ed etano:
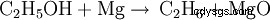
Quando il magnesio brucia nell'aria, reagisce con l'ossigeno per formare ossido di magnesio:
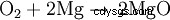
Prove individuali
- ↑ ChemDat di Merck, versione 2.13.2, 2005
