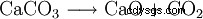| formula strutturale | |||||||
|---|---|---|---|---|---|---|---|
| Nessuna formula strutturale disponibile | |||||||
| Generale | |||||||
| Nome | Ossido di calcio | ||||||
| Altri nomi |
| ||||||
| Formula molecolare | CaO | ||||||
| Numero CAS | 1305-78-8 | ||||||
| Breve descrizione | polvere bianca | ||||||
| Proprietà | |||||||
| Massa molare | 56,08 g mol | ||||||
| Stato della materia | risolto | ||||||
| Densità | 3,37 g cm (20 °C)> | ||||||
| Punto di fusione | 2570-2580 °C | ||||||
| Punto di ebollizione | 2850 °C (100 mbar) | ||||||
| Pressione di vapore | non applicabile | ||||||
| Solubilità | appena in acqua, 1,65 g l (a 20 °C), reazione violenta | ||||||
| Istruzioni di sicurezza | |||||||
| |||||||
| MAC | sollevato | ||||||
| Ove possibile e comune, vengono utilizzate le unità SI. Salvo diversa indicazione, i dati forniti si applicano a condizioni standard. | |||||||
ossido di calcio (anche calce bruciata , calce viva , calce viva o calce ) è una polvere bianca che reagisce con l'acqua con lo sviluppo del calore. La reazione produce idrossido di calcio (calce spenta ) formato:
Quicklime è Softburned e indurito distinto.
Produzione
- Articolo principale: Ciclo tecnico a calce
Su scala industriale, l'ossido di calcio è prodotto dalla combustione della calce. Da una temperatura di circa 800 °C, il calcare (carbonato di calcio) viene disacidificato, cioè viene espulsa anidride carbonica e si forma ossido di calcio.
Si distingue tra calce cotta, tra l'altro, la velocità con cui la calce reagisce con l'acqua (il cosiddetto processo di spegnimento):
<2 min tempo di reazione:calce morbida
Tempo di reazione 2 - 6 min:calce viva
> 6 min tempo di reazione:calce viva
Tuttavia, non esistono definizioni precise.
Le differenze nella velocità di reazione sono una conseguenza della dimensione dei cristalliti del CaO, del volume dei pori e della superficie specifica, che sono influenzati dalla temperatura e dalla durata della cottura.
Calce tenera bruciata prodotto a temperature di 900-1000 °C, calce cotta dura fino a 1400 °C, per cui solitamente ha un ruolo anche la durata dell'effetto della temperatura.
Quando sono sufficienti quantità minori (scala di laboratorio), si può ottenere ossidando il calcio.
L'ossido di calcio reattivo si ottiene decomponendo termicamente l'idrossido di calcio, che si decompone a 550 °C a pressione atmosferica in ossido di calcio e acqua. L'ossido di calcio formato in queste condizioni non è molto cristallino, quindi è altamente reattivo.
La calce viva (rapido) e la grassello di calce (idrossido di calcio) sono altamente corrosivi (pH 12-13), il contatto con gli occhi può causare cecità!
Utilizzo
La calce viva viene utilizzata nel settore edile come additivo alla malta ed è anche un componente minore del clinker di cemento. In chimica, la sostanza viene utilizzata anche come agente essiccante. Altri campi di applicazione della calce bruciata sono ad es. B. fertilizzante a base di calce, per la produzione di carburo di calcio e per la produzione di malte di calce, intonaci a base di calce e pitture a base di calce e da utilizzare come neutralizzante.
Una delle principali aree di applicazione è la desolforazione della ghisa, dove lo zolfo [S] si presenta come compagno [FeS] e deve essere sciolto nel percorso verso l'acciaio (convertitore).La calce (CaO) viene soffiata nella ghisa o con un mescolatore mescolato. La calce si combina con lo zolfo per formare solfuro di calcio [CaS] e sale in superficie dove si deposita come scoria. Questo viene rimosso con una raschiatrice dopo la desolforazione.
L'ossido di calcio è un'applicazione importante come precursore nella produzione di idrossido di calcio mediante aggiunta di acqua (calce spenta o calce spenta ).
La grassello di calce viene utilizzata, tra l'altro, come alternativa al calcare nella desolforazione dei fumi. La quantità utilizzata qui è circa 1,8 volte inferiore rispetto al calcare. Il gesso (solfato di calcio) ottenuto dalla calce viva ha un grado di bianco dell'80% e può essere utilizzato commercialmente. Data la sua elevata reattività, sono richieste quantità di consumo inferiori. Lo svantaggio è il suo prezzo significativamente più alto rispetto al calcare.
La calce di cloro può essere prodotta dall'idrossido di calcio mediante ulteriori reazioni.
Viene aggiunto agli alimenti come correttore di acidità. Viene utilizzato principalmente come cosiddetto coadiuvante tecnico che non è più presente negli alimenti finiti.Nell'UE è classificato come additivo alimentare con la denominazione E 529 senza limite massimo (quantum satis ) generalmente approvato per gli alimenti.
Fonti
- ↑ Voce su ossido di calcio nel database delle sostanze GESTIS della BGIA, recuperato il 4 ottobre 2007 (JavaScript richiesto)
- ↑ Scheda di sicurezza dei materiali (Merck)